双特异性抗体(bispecific antibody,BsAb)能够发挥两种单抗的协同作用,在临床前研究和临床治疗上可能比混合使用两个单抗更有优势,已经成为抗体药物研发领域的一个重要分支,也是当下制药行业最热门的研发和投资方向之一。根据相关信息统计,目前全球有超过180种双特异性抗体处于临床开发阶段,约260种双特异性抗体处于临床前开发阶段。
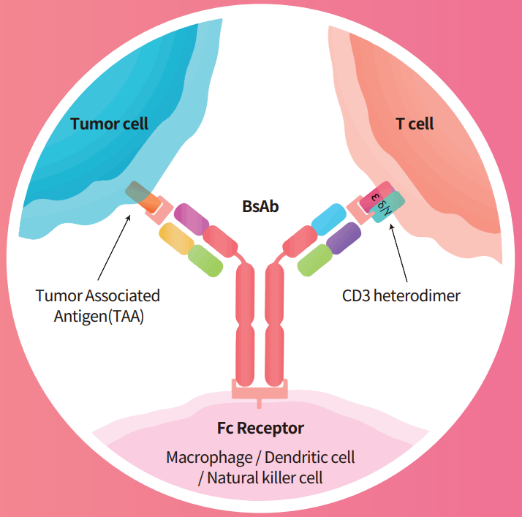
CD3+双特异性T细胞重定向在肿瘤治疗中的作用机制
靶向CD3抗原的双特异性抗体是一类能够将T细胞与肿瘤细胞在空间上拉近,利用T细胞对肿瘤细胞的杀伤性作用治疗血液和实体肿瘤的抗体疗法,这类抗体被称为T细胞衔接器(T cell-engaging bsAb, TCE双抗)。在临床阶段的双特异性抗体中,有接近一半的候选物靶向CD3抗原,因此TCE双抗的开发是双特异性抗体领域的主流热点。
2021年4月7日,CDE官网显示辉瑞公司的anti-BCMA/CD3双特异性抗体药物Elranatamab(PF-06863135)的临床试验申请已获国家药监局受理,用于治疗多发性骨髓瘤。但仅1个月后,辉瑞公司在5月4日的公告中称,由于Elranatamab 在注册性Ⅱ期临床试验(NCT04649359)中发生3例外周神经损伤事件,该临床试验宣告暂停患者招募。辉瑞Elranatamab双特异性抗体的临床突发事件,让我们不得不在面对TCE双抗药物研发的热潮前冷静下来,对TCE双抗的安全性和有效性进行更加谨慎地思考和评估。
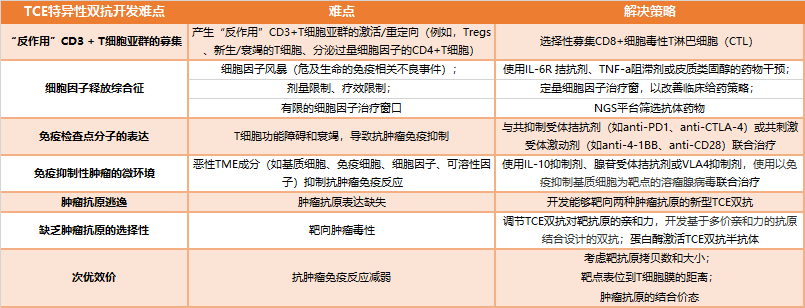
目前,已经有约100项临床试验研究TCE双抗的安全性和有效性。虽然相关研究取得了一定进展,但仍存在许多挑战。近日,强生公司在《The British Journal of Cancer》杂志上发表文章《Overcoming the challenges associated with CD3+ T-cell redirection in cancer》,探讨了靶向CD3双特异性抗体的开发中所面临的关键挑战以及达到平衡抗肿瘤活性和安全性的方案。该文章列出TCE双抗研发人员需要考虑的因素,下文将一一进行解读。
TCE双抗通过将所有T细胞亚群重新定向到癌细胞来发挥有效的肿瘤细胞杀伤。然而,多克隆T细胞活化和重定向存在一些缺点,如具有“反作用”的CD3+T细胞亚群的募集,这些细胞亚群包括初始/衰竭T细胞、调节性T细胞(TREG)和其他CD4+T细胞等。事实上,已经有关于双特异性抗体Blinatumomab(Blincyto®)耐药性的报道,这是由于CD3+ CD4+ CD25hl FoxP3+ TREG细胞的激活与募集可抑制T细胞增殖并阻碍CD8+介导的肿瘤细胞裂解,从而影响Blinatumomab治疗前体B-ALL患者的疗效。所以通过提高T细胞结合双特异性抗体的选择性,可以更有效的发挥T细胞的抗肿瘤免疫应答,可通过选择性募集CD8+细胞毒性T淋巴细胞(CTL)来实现这一目标。
细胞因子释放综合征是一种严重的免疫反应,其诱发原因是TCE双抗不加区别地结合所有T细胞,导致全身迅速释放促炎性细胞因子。这些核心细胞因子水平的升高会诱导免疫细胞产生过量额外的细胞因子,从而引发称为“细胞因子风暴”的放大现象。
用药理学方法治疗细胞因子释放综合征是个良好的解决办法:
◊ 激活T细胞后产生的TNF-α能够介导单核细胞活化,是anti-HER2/CD3 双抗治疗后细胞因子释放的主要来源,可使用TNF-α阻断剂抑制细胞因子的释放。
◊ 使用免疫抑制剂地塞米松、或用抗IL-6受体抑制剂Tocilizumab进行预治疗。
◊ 设计定量细胞因子模型以改进临床给药策略,在达到疗效的同时可将毒性降至最低。
通过二代测序(NGS)抗体发现平台,可从人源化大鼠中筛选出结合CD3不同表位、亲和力有差异的CD3抗体,与肿瘤靶点抗体进行组合后可以开发出大量的TCE双抗候选物:
◊ 例如anti-BCMA/CD3 TCE双抗在小鼠异种移植模型中诱导了强有力的肿瘤抗原特异性杀伤,并且几乎检测不到细胞因子的释放。
◊ 在T细胞或肿瘤细胞表面表达的抑制性免疫检查点分子如PD-1、PD-L1、CTLA-4、TIM3等可以引发T细胞功能障碍和衰竭,从而抑制抗肿瘤免疫反应。可联合使用共抑制受体拮抗剂(如anti-PD1、anti-CTLA-4)进行治疗。
◊ 激动性抗体能够激活T细胞上的共刺激受体,增强抗肿瘤免疫反应,如肿瘤坏死因子受体(TNFR)和免疫球蛋白。可联合使用共刺激受体激动剂(如anti-4-1 BB, anti-CD28)进行治疗。
恶性TME包括:抗肿瘤免疫细胞和间质细胞,如肿瘤相关成纤维细胞(CAFs)、Treg细胞、骨髓源性抑制细胞(MDSCs)和肿瘤相关巨噬细胞(TAMs),以及免疫抑制细胞因子和可溶性因子:如腺苷、IL-10、TGF-P和IDO。
破坏实体瘤周围的反应性基质是提高TCE 双抗抗肿瘤活性的一种策略,具体方法包括:
提高肿瘤抗原的特异性,是开发TCE双抗的另一个挑战。正常细胞上的低水平抗原表达可能导致有害的靶外肿瘤毒性,其中CD3+T细胞的细胞溶解活性直接作用于健康组织。
◊ 开发依赖蛋白酶激活的TCE双抗
◊ 临床前研究表明,调节CD3+双特异性T细胞对靶抗原的亲和力是实现抗肿瘤活性和安全性最佳平衡的合理途径:
开发基于多价亲和力的抗原结合设计的双抗,如anti-CD3 X anti-HER2双特异性抗体。这种双抗的两条低亲和性的anti-HER2抗体链可结合HER2过表达的肿瘤细胞,具有比健康组织更高的抗原亲和性,由此CD3+T细胞可实现选择性重定向至HER2癌细胞。
◊ 另外,研究描述了一种新的分裂T细胞结合抗体形式—称为半抗体,可避免CD3+T细胞重定向相关的靶向毒性:
两个互补的半抗体与各自的抗原同时作用于单个靶细胞,激活CD3结合位点,并重新定向CD3+T细胞至肿瘤细胞。这样可以选择性杀伤双抗原阳性的肿瘤细胞,同时保留表达单一抗原的细胞。可选择性杀伤双抗原阳性的肿瘤细胞,同时保留表达单一抗原的细胞。
TCE双抗抗肿瘤活性受到如下4种因素的影响,在TCE双抗设计开发时需要同时考虑这4种因素:
◊ 肿瘤靶点抗原的大小:有临床前数据表明,TCE双抗对表达小抗原肿瘤细胞的杀伤活性要高于表达大抗原的肿瘤细胞。
◊ 靶点表位到T细胞膜的距离:有临床前数据表明,靶向CSPG4近膜区的anti-CSPG4/CD3 TCE双抗杀伤肿瘤效果要好于靶向CSPG4远膜区的anti-CSPG4/CD3 TCE双抗
◊ 肿瘤抗原的拷贝数
◊ 肿瘤抗原的结合价态
TCE双抗药物的开发仍面临着许多挑战,如何在增强双抗抗肿瘤活性的同时尽量减少毒性,是每一位TCE双抗开发者需要思考的问题。上述文章内容应该对平衡TCE双抗抗肿瘤活性和安全性具有重要的意义。
为助力TCE双抗的研发,ACROBiosystems开发了CD3δ/ CD3ε, CD3γ/ CD3ε系列靶点抗原,加速抗体药物的开发进程。
◊ 产品特点:
◊ 应用场景:
-
TCE双抗的免疫 & 筛选
-
TCE双抗的质控
-
临床血药浓度分析
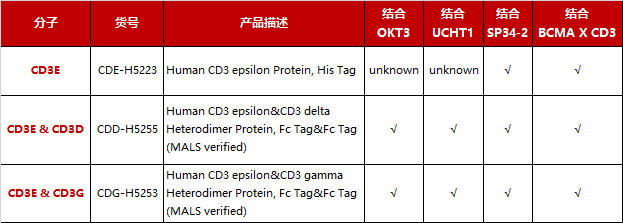
经实验验证,上述3种抗原蛋白与OKT3、SP34-2、UCHT1、TCE双抗等热门抗体的结合活性良好。
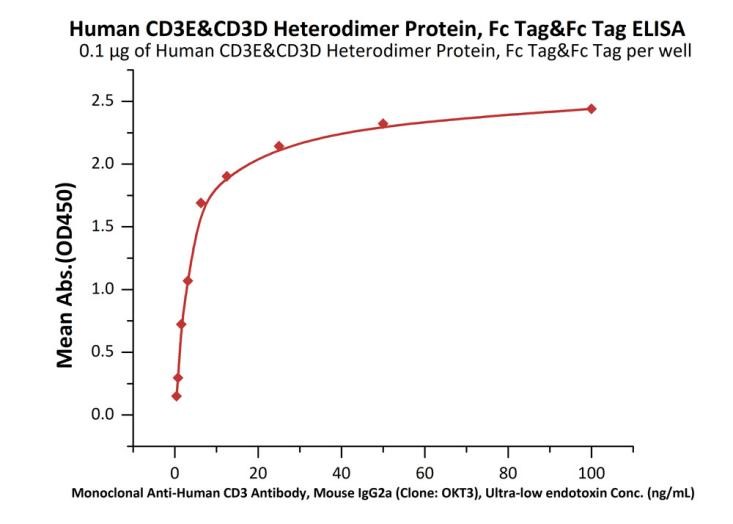
Immobilized Human CD3E&CD3D Heterodimer Protein, Fc Tag&Fc Tag (Cat. No. CDD-H5255) at 1 μg/mL (100 μL/well) can bind Monoclonal Anti-Human CD3 Antibody, Mouse IgG2a (Clone: OKT3), Ultra-low endotoxin (Cat. No. CDE-M120a) with a linear range of 0.8-6 ng/mL (QC tested).
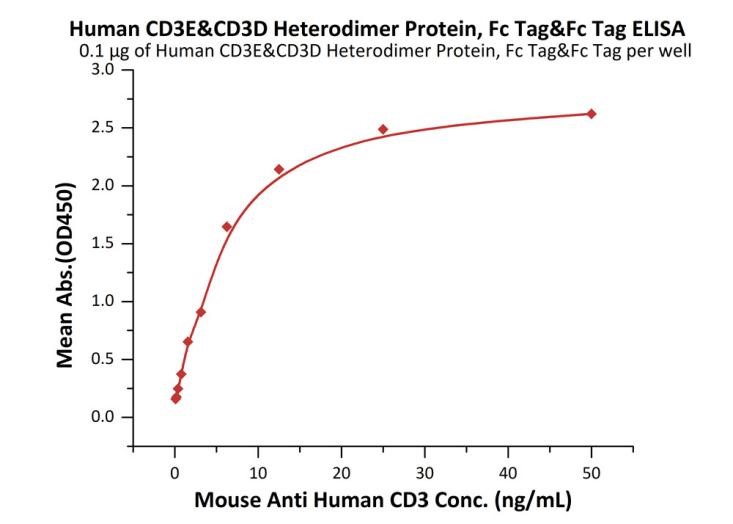
> CDD-H5255 & SP34-2
Immobilized Human CD3E&CD3D Heterodimer Protein, Fc Tag&Fc Tag (Cat. No. CDD-H5255) at 1 μg/mL (100 μL/well) can bind Mouse Anti Human CD3 with a linear range of 0.8-6 ng/mL (Routinely tested).
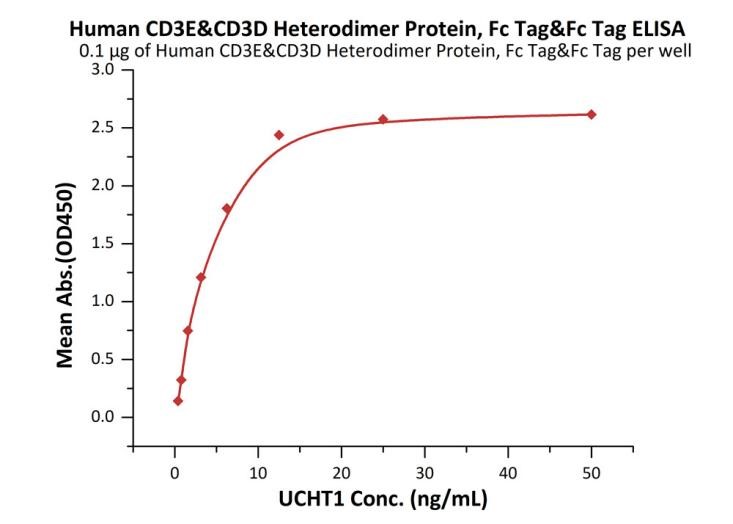
> CDD-H5255 & UCHT1
Immobilized Human CD3E&CD3D Heterodimer Protein, Fc Tag&Fc Tag (Cat. No. CDD-H5255) at 1 μg/mL (100 μL/well) can bind UCHT1 with a linear range of 0.8-3 ng/mL (Routinely tested).
> CDD-H5255 & BCMA×CD3
Immobilized Human CD3E&CD3D Heterodimer Protein, Fc Tag&Fc Tag (Cat. No. CDD-H5255) at 1 μg/mL (100 μL/well) can bind Bispecific BCMA×CD3 T cell-engaging Antibody with a linear range of 0.8-6 ng/mL (Routinely tested).
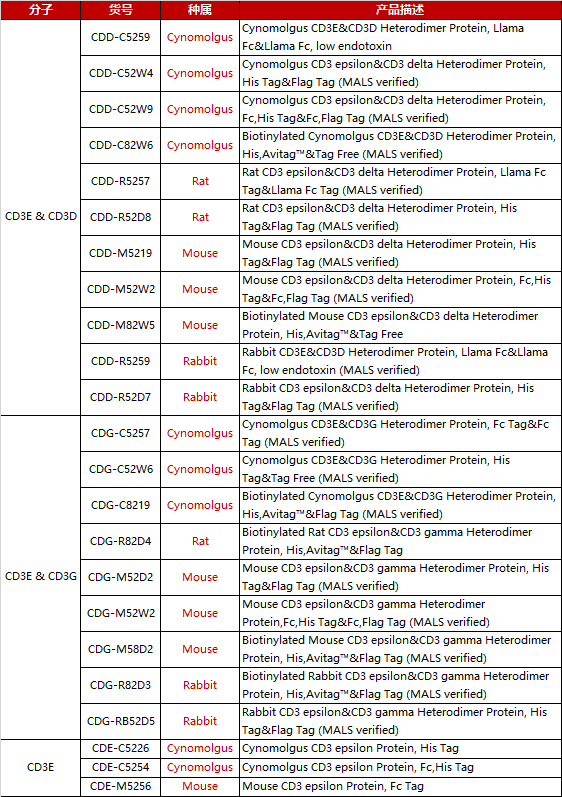
此外,ACROBiosystems还开发出一系列非人源种属齐全的CD3蛋白,可供TCE双抗开发者进行种属交叉性实验。
参考文献
Ajit Singh , Sundee Dees,Iqbal S. Grewal.Overcoming the challenges associated with CD3+ T-cell redirection in cancer[J]. British Journal of Cancer (2021) 124:1037–1048.
您可通过以下方式联系到ACROBiosystems:
邮件:inquiry@acrobiosystems.com
电话:15117918562
微信:扫描下方二维码即可进行沟通

(请备注公司+姓名)




















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!

































 膜杰作
膜杰作 Star Staining
Star Staining