癌细胞在复杂的微环境中发展和增殖,常常会导致异质疾病甚至是患者死亡。虽然基于抗体的治疗在实体肿瘤患者的临床治疗中得到了广泛的应用,但其疗效仍有待提高。抗体在实体瘤的局限性主要是由于其体积大,在实体组织中渗透能力差。
大约30年前,人们在骆驼(单峰骆驼/dromedaries、骆驼/camels、羊驼/llamas、大羊驼/guanacos和小羊驼/vicuñas)的血清中偶然发现了功能性重链抗体。这种重链抗体的可变域包括完整的抗原结合潜力,与同源抗原的强亲和性,因此它被认为是最小的自然发生的完整的抗原结合片段。基于重链抗体,Ablynx公司(2018年被赛诺菲收购)开发了仅含有VHH片段的抗体,因其纳米级的微小尺寸激发了Ablynx提出“Nanobody(纳米抗体)”这个概念。
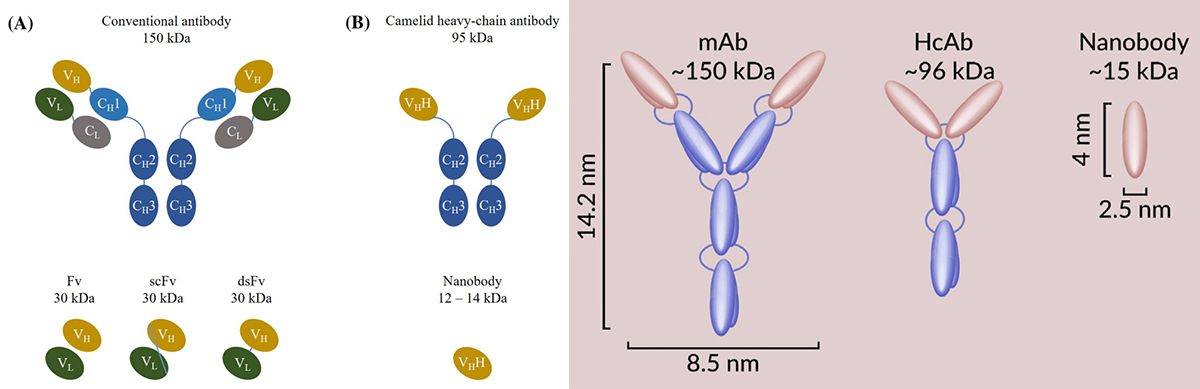
mAb、重链抗体、Nanobody等不同抗体结构
看到这是不是不由自主的想到了我们可爱的羊驼玩偶!别着急,文末有惊喜哦~
Nanobody是一种新颖独特且完整的抗原结合片段,结构简单,分子量小(约15 KDa, 大约比单克隆抗体小10倍),具有物理和化学稳定性好,水溶性好,组织渗透能力强,可穿透血脑屏障,来源自然等优点。Nanobody可通过重组微生物高效生产,成本较低,易于组装或合并成更复杂的多能结构。兼具了传统抗体与小分子药物的优势的Nanobody,几乎完美克服了传统抗体的开发周期长、稳定性较低、保存条件苛刻等缺陷,逐渐成为了新一代治疗性生物医药与临床诊断试剂中的新兴力量。
Nanobody的一个相当大的缺点是它们在血液中被快速清除,这导致药物的半衰期太短。针对半衰期较短的问题,可利用蛋白类药物的长效平台技术,主要包括两种策略:
基于以上两种策略,目前较为成熟的技术包括聚乙二醇(PEG)修饰、人血清白蛋白(HSA,Human Serum Albumin)融合、Fc融合等。PEG修饰是通过引入亲水性PEG链状分子,增加水力学半径,延长药物半衰期;白蛋白融合或Fc片段融合是借助pH依赖的FcRn再循环途径延长药物半衰期(点击查看FcRn介导延长半衰期的机制)。
除了以上较为成熟的技术外,一些新兴技术正逐渐从幕后走向台前,如融合与白蛋白结合的多肽段-ABD融合等;融合惰性蛋白增大分子量——XTEN融合;引入糖基化修饰位点——CTP 融合等。
HSA是一种主要用于药物传递和疾病诊断的治疗性蛋白。Nanobody与HSA的融合,可以增加药物的半衰期,提高药物疗效。
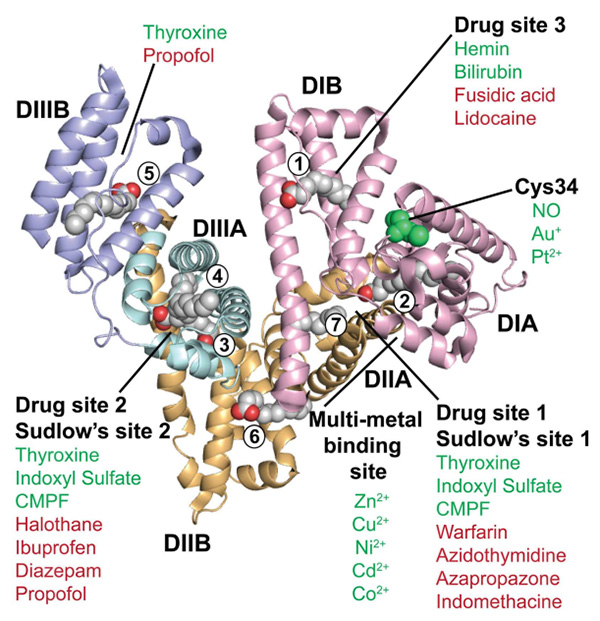
HSA的结晶结构
HSA的X射线晶体结构显示,它是一个心形分子,含有585个氨基酸,它主要由α -螺旋结构构成,缺乏β -折叠,组合成三个同源域DI, DII和DIII,其中每个被分为A和B子域 (DIA, DIB, DIIA, DIIB, DIIIA和DIIIB),这些域由长而柔性的环连接。HSA是H血浆中的主要蛋白,其浓度约为45 mg/ml (0.6 mM),循环半衰期为20天。Ablynx独家的半衰期延长技术正是将Nanobody与血清白蛋白结合,提升双抗分子量并借助 FcRn的再循环作用,将半衰期由数小时延长至3周以上。
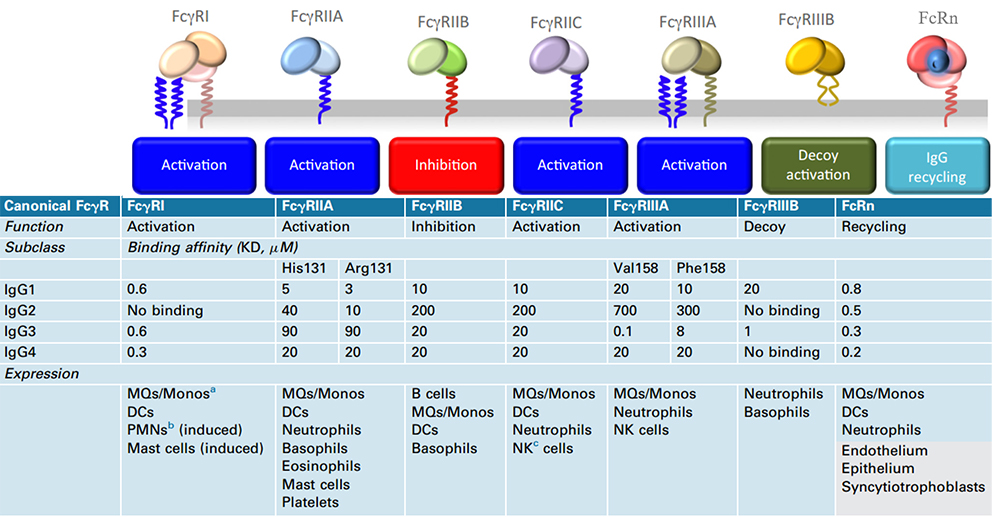
同时,Nanobody除了半衰期短,由于缺乏单克隆抗体的Fc片段,不具备Fc介导的效应功能,如用于抗肿瘤治疗,缺乏Fc带来的抗体依赖的细胞介导的细胞毒(ADCC)效应和血清稳定性。自然杀伤细胞(NK)是介导ADCC作用的主要免疫细胞,其细胞表面的Fc受体FcγRIIIa(CD16a)在识别和结合Fc中起关键作用。
Nanobody可以很容易地配备Fc区域(铰链、CH2和CH3结构域)重组人源化重链抗体形式,以实现包括Fc介导的效应因子功能,并增加血液滞留时间,但也将不可避免地降低其扩散优势。选择Fc融合片段,更倾向于选择IgG1 Fc,这和IgG1与Fc受体蛋白的亲和力结合特性有关。
Fc受体与各种IgG亚类结合亲和性与在细胞中的表达
如下表所示,FDA已经批准了的融合Fc的药物,都含有人IgG1 Fc结构域,其主要目的是延长活性部分的血清半衰期。
已获FDA批准的融合Human IgG1 Fc的部分药物

除了提高血清半衰期,Fc融合还改善了药物的稳定性和溶解性,并且对于生产过程是有利的,因为Fc的融合表达,利于Protein A的亲和纯化,进而简化蛋白药物的下游纯化流程。因此,Fc融合蛋白在获得批准的产品数量、在不同疾病领域的应用以及全球价值方面都取得了相当大的成功。
抗体是用于靶向治疗的主要大分子,可显著改善癌症患者的临床护理和生活质量。然而,抗体在大小、不完全肿瘤渗透和可能的免疫原性方面的局限性导致了新一代小药物和药物的发展。
Nanobody不仅为癌症的治疗提供了新的可能性,而且还在亚细胞水平上为各种人类疾病提供了新的治疗可能性,这将使生物医学领域发生革命性的变化。由于体积小且对组织渗透性好,可能成为理想的诊断和治疗工具。但也因缺乏功能性Fc,血清半衰期非常短,在肾脏清除率很快。
HSA和Fc融合技术为有治疗价值的蛋白质和多肽赋予更类似抗体的特性,目前纳米抗体正广泛应用于包括炎症、传染病和血液学的临床开发及治疗领域。对于慢性疾病适应症,Nanobody延长暴露是至关重要的,可以通过融合HSA或Fc产生半衰期延长的结构;而在急性适应症中,非半衰期延长的形式可能显示出更强的动力学的优势。
除了融合HSA,引入抗HSA或抗FcR的Nanodody,介导药物与HSA的结合也可以有效提高药物的半衰期。目前已经报道了一系列基于抗肿瘤抗原、抗CD16和抗HSA纳米体的双特异性纳米体。
诚然,合理的药物设计可为Nanobody加码,使其充分彰显潜力。
ACROBiosystems可为您提供如下系列产品:
热门靶点蛋白产品,用于免疫、筛选、工艺方法开发及优化;
结构均一、活性经验证、严格质控的HSA和IgG Fc产品——满足开发融合HSA和Fc功能验证和方法开发环节对于对照产品的需求;如研发抗HSA的Nanobody药物,HSA可作为结合配体使用;
全系列高质量Fc受体蛋白:FcRn、FcγRI/CD64、FcγRIIA/CD32a、FcγIIB/CD32b、FcγRIIIA/CD16a、FcγRIIIA/CD16b——用于融合Fc的Nanobody药物的半衰期和与Fc受体蛋白的结合亲和力验证。
ACROBiosystems开发的SA蛋白序列是仅去除信号肽和前肽的天然完整序列;
产品丰富:覆盖Human、Mouse、Cynomolgus、Rabbit种属;
纯度高:经SDS-PAGE验证纯度>95%,经SEC-MAL验证纯度>90%;
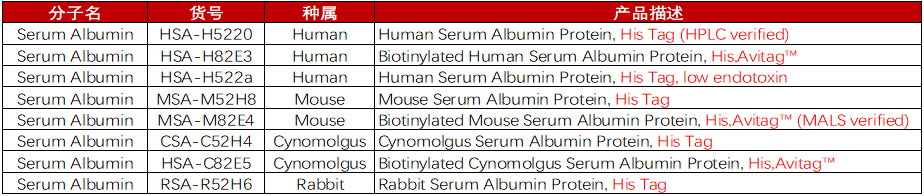 点击图片内容查看产品详细信息
点击图片内容查看产品详细信息
> 经还原条件下SDS-PAGE验证,人血清白蛋白 (Cat.No.HSA-H5220) 纯度高于95%;经SEC-MALS验证,人血清白蛋白 (Cat.No.HSA-H5220) 纯度高于90%,分子量为65-75kDa。
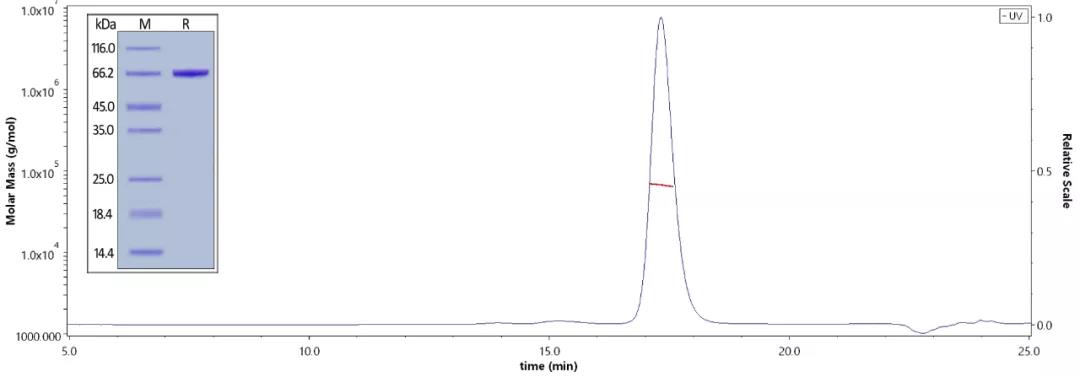
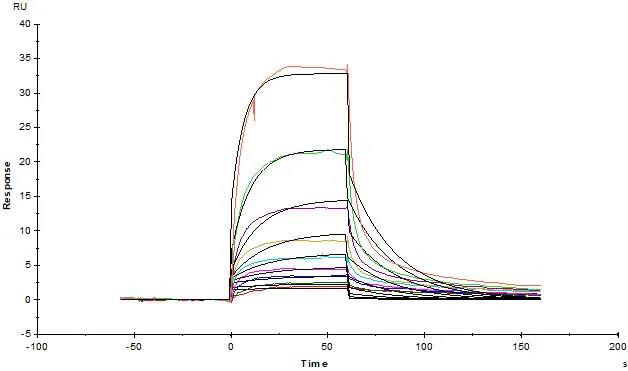
> 经SPR验证,固定在CM4芯片上的人血清白蛋白,His tag (Cat.No.HSA-H5220) 可以与人FcRn异质二聚体蛋白,His tag (Cat.No.FCN-H52W7) 结合,亲和力常数为0.381 μM(Biacore T200)。
IgG Fc

IgG Fc用途是什么?
作为IgG抗体及融合Fc片段的Nanobody的同型对照,应用于抗体筛选、功能验证等场景。
IgG Fc 同型对照作用,如何实现?
重组蛋白IgG Fc包含了铰链区,CH2,CH3,而不包含Fab序列,因此可以作为对照,明确您抗体的Fab识别靶抗原的特异性作用。
更多产品选择:覆盖Human IgG1 Fc、IgG2 Fc、IgG3 Fc、IgG4 Fc;Mouse IgG1 Fc、IgG2a Fc、IgG2b Fc;Llama IgG2b Fc;Rabbit的IgG Fc;
HEK293细胞表达,实现翻译后糖基化等修饰及蛋白正确折叠;
不同标签,满足不同应用场景需求:Tag Free、AvitagTM、His Tag、gD Tag、Flag Tag、AvitagTM &His tag;
高纯度:经SDS-PAGE验证纯度>95%;经SEC-MAIL验证纯度高于90%;
 点击图片内容查看产品详细信息
点击图片内容查看产品详细信息
> 经还原条件下SDS-PAGE验证,人源IgG1 Fc, Tag Free (Cat.No.FCC-H5214) 纯度高于95%;经SEC-MALS验证,人源IgG1 Fc, Tag Free (Cat.No.FCC-H5214) 纯度高于90%,分子量为50-65kDa(二聚体)。

> 经ELISA验证,人源CD64, His Tag (Cat.No.FCA-H52H1) 可与人源IgG1 Fc, Tag Free (Cat.No.FCC-H5214) 特异性结合,线性区间为1-16 ng/mL。

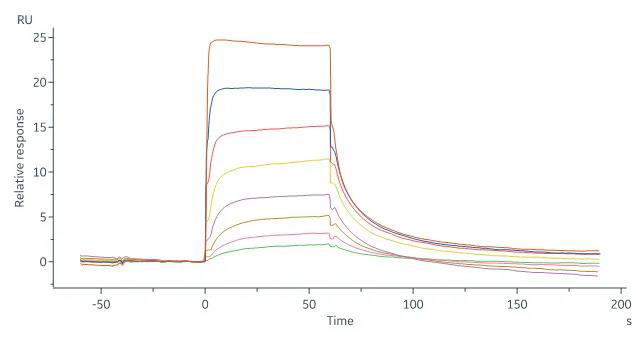
> 经SPR验证,人源FCGRT&B2M异源二聚体蛋白, His Tag (Cat.No.FCN-H52W7) 可以通过捕获在CM5芯片上的抗anti-His 抗体与人源IgG1 Fc, Tag Free (Cat.No.FCC-H5214) 特异性结合,亲和力常数为0.957 μM (Biacore 8K)。
即日起至10月31日,购买IgG Fc或SA,即可拥有ACRO超级软萌的羊驼玩偶。快来填写表单申请吧!

参考文献:
1. Ivana Jovčevska1, Serge Muyldermans. The therapeutic potential of nanobodies.BioDrugs.2020, 34: 11–26
2. Elmira Karami, Mahdi Behdani, et al. Albumin nanoparticles as nanocarriers for drug delivery: Focusing on antibody and nanobody delivery and albumin-based drugs. Journal of Drug Delivery Science and Technology. 2020, 55: 1014713. Zhimin Xu, Chuangnan Qiu, et al. Abispecific nanobody targeting the dimerization interface of epidermal growth factor receptor: Evidence for tumor-suppressive actions in vitro and in vivo. Biochemical and Biophysical Research Communications. 2021, 548: 78-83
4. Kine Marita Knudsen Sand, Malin Bern, et al. Unraveling the interaction between FcRn and albumin: opportunities for the design of albumin-based therapeutics.Frontiers in Immunology. 2015, 5, 6825. Alain Beck, Janice M. Reichert. Therapeutic Fc-fusion proteins and peptides as successful alternatives to antibodies. Landes Bioscience.2011,3(5): 415-4166. Liming Liu. Pharmacokinetics of monoclonal antibodies and Fc-fusion proteins. Protein Cell. 2018, 9(1): 15–32
7. Ditza Levin1, Basil Golding, et al. Fc fusion as a platform technology: potential for modulating immunogenicity. Trends in Biotechnology. 2015, 33(1): 27-34



























 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!


























 膜杰作
膜杰作 Star Staining
Star Staining























