虽然在多发性骨髓瘤(MM)的治疗中,单抗、CAR-T细胞治疗,ADC药物等治疗策略,已经取得了许多进展,其早期临床结果似乎很有前景,但总体生存曲线仍然没有平台期,最终大多数患者会发展为进展性疾病,如治疗期间MM表面靶点表达的异质性以及丢失等现象。双特异性抗体是一种新的免疫治疗方法,旨在结合恶性浆细胞和细胞毒性免疫效应细胞(T细胞/自然杀伤细胞NK细胞)表面抗原,以创建免疫突触,导致T/NK细胞激活和恶性浆细胞的破坏。
尽管MM的新型治疗通常在已用尽大多数或所有可用治疗的患者中进行研究,但双特异性药物进入早期治疗线的可能性很大,并在不久的将来,双特异性药物可能会成为MM治疗模式的一个重要组成部分,大有可为。

MM免疫治疗的双特异性和三特异性抗体靶点
(填充色表示靶抗原的功能等级,填充强度表示转化发生阶段:临床/颜色较深;临床前/颜色较浅)
由于许多MM患者无法接受多线治疗,无论是由于合并症、治疗毒性或早期死亡,每一线连续治疗的缓解时间均较短。T细胞功能下降是MM治疗和衰老的结果,有证据表明T细胞耗竭是MM复发的显著特征。因而有必要利用T细胞重定向治疗,在治疗过程的早期实现深度和持久的缓解。鉴于高应答率、深度应答、应答的潜在持久性,相比于CAR-T疗法,毒性有限且便于给药,双抗可能在前期或早期复发中有效。
目前,已经开发出有或无Fc区域的双抗。缺乏Fc区域的分子由于体积小而容易穿透肿瘤,但由于其半衰期短,需要频繁或持续的输注;带有Fc区域的双抗已被证明具有较长的半衰期,可以降低给药频率。因此,正在进行的I期和II期试验中的所有双抗都在其抗体结构中包含了Fc区域。目前大部分双抗的研究都针对T细胞上的CD3。临床前实验也在研究NK细胞(NKp30或NKG2D)参与作为一种新的作用机制,并获得早期成功。此外,目前正在临床前研究的三特异性抗体试图添加T细胞共刺激蛋白以减少T细胞无效或在接触NK细胞时靶向双重骨髓瘤抗原。

MM免疫治疗的双特异性和三特异性抗体结构
A.靶向骨髓瘤细胞表面抗原和T/NK细胞的双抗;B.缺少Fc部分的双抗;C.靶向免疫效应细胞和两种不同骨髓瘤抗原的三特异性抗体;D.与共刺激免疫效应细胞增强细胞毒性的三特异性抗体。
为了最大限度地提高疗效和降低毒性,双/三特异性抗体应该靶向一种针对MM细胞的特异性抗原,并且在其他健康组织中表达最少。GPRC5D是一种功能未知的G蛋白偶联孤儿受体。在正常组织中,GPRC5D仅在毛囊等产生硬角质蛋白的细胞表面表达(包括毛干、指甲和舌头中央区域),而在MM细胞表面GPRC5D特异性高表达。对人骨髓样本 RNA 表达数据的分析表明,原发性恶性浆细胞表达的 GPRC5D mRNA 比外周血中B细胞表达的多 1000 倍。并且GPRC5D 的高表达与MM预后不良有关。因此,GPRC5D是治疗MM的潜在优秀靶点。
GPRC5D分布与BCMA相似,但独立于BCMA,靶向MM表面GPRC5D的抗体,在BCMA抗原逃逸模型中也表现出很好的疗效。抗GPRC5D可导致MM细胞系和原代MM细胞毒性,诱导细胞因子释放,体内活性可与抗BCMA 相媲美。因此,GPRC5D 免疫治疗在治疗晚期MM显示出巨大的潜力。
潜在的脱发可能是患者可以接受的风险,然而,毛囊被认为是一个免疫特权部位,这也解释了,在食蟹猴和小鼠中用物种交叉反应性 CAR-T细胞治疗后的小鼠明显缺乏皮肤或毛发毒性,进一步证明GPRC5D是一个有吸引力的免疫治疗靶点。
截至目前,靶向治疗MM的双抗试验至少有17个,大部分处于临床I/II期,涉及4个不同的抗原靶点,所有这些研究都针对T细胞上的CD3。其中靶向GPRC5D的双抗是由强生公司开发的靶向GPRC5D和CD3E的Talquetamab/JNJ-64407564,通过激活T细胞,诱导T细胞对GPRC5D阳性MM细胞进行杀伤。

Talquetamab作用机制示意图
Talquetamab开展的全球临床试验

双抗,CD3×GPRC5D双抗,代表了MM治疗的一个有希望的策略,并可能在不久的将来整合到MM的治疗模式。当然,仍有许多未解答的问题和未探索的机会。比如,耐药性的机制目前还不清楚,值得进一步研究,以了解各种双特异性药物的合理排序/组合。
ACROBiosystems为助力双特异性抗体开发,可提供“膜杰作”——全长GPRC5D蛋白和CD3系列蛋白。

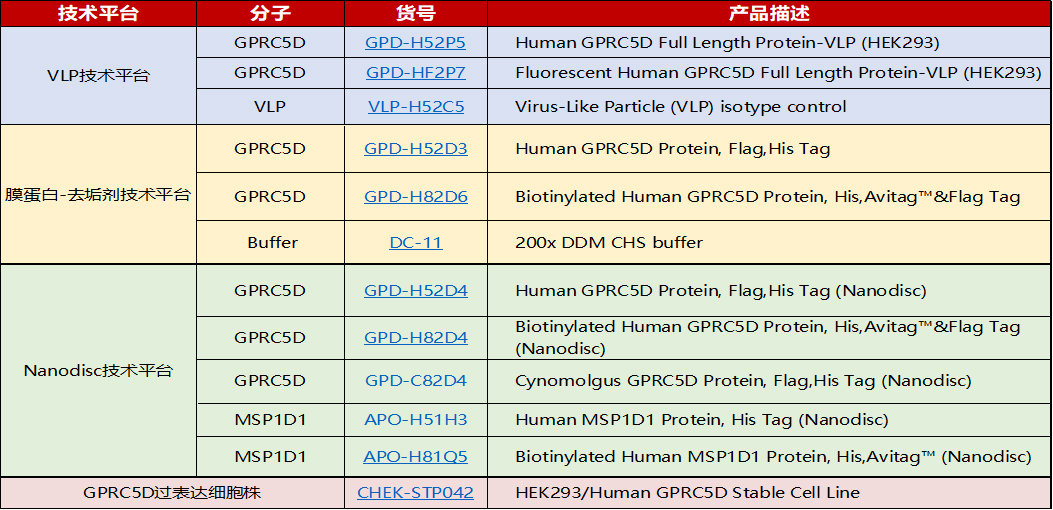
ACROBiosystems拥有全长多次跨膜蛋白平台化解决方案,可提供VLP、去垢剂、Nanodisc三种版本的全长七次跨膜蛋白GPRC5D,具有天然完整构象,高生物活性经Anti-GPRC5D抗体结合验证,满足更多应用场景需求,全面助力GPRC5D靶向药物及疗法研发。

Human GPRC5D-VLP (Cat. No. GPD-H52P5)可与Anti-GPRC5D 抗体(Human IgG4)特异性结合,线性区间为0.2-25 ng/mL。

Fluorescent Human GPRC5D Full Length Protein-VLP (Cat. No. GPD-HF2P7) 可与Anti-GPRC5D抗体(Human IgG4)特异性结合, 线性区间为0.4-25 ng/mL。

生物素化Human GPRC5D, His,Avitag&Flag Tag (Cat. No. GPD-H82D6)可与Anti-GPRC5D 抗体特异性结合,线性区间为0.001-0.25 μg/mL。

生物素化Human GPRC5D-Nanodisc (Cat. No. GPD-H82D4)可与Anti-GPRC5D 抗体(Mouse IgG1)特异性结合,线性区间为0.002-0.313 μg/mL。

 CD3全系列靶点蛋白:CD3E(CD3ε)、CD3D(CD3δ)、CD3 G(CD3γ)、CD3E&CD3D (CD3ε&CD3δ)、CD3E&CD3G (CD3ε& CD3γ)
CD3全系列靶点蛋白:CD3E(CD3ε)、CD3D(CD3δ)、CD3 G(CD3γ)、CD3E&CD3D (CD3ε&CD3δ)、CD3E&CD3G (CD3ε& CD3γ)
 His,His&Avi,Fc,Llama Fc,Flag等多标签设计
His,His&Avi,Fc,Llama Fc,Flag等多标签设计
 Human、Mouse、Rat、Rabbit、Cynomolgus等多种属选择
Human、Mouse、Rat、Rabbit、Cynomolgus等多种属选择
CD3E&CD3D、 CD3E&CD3G,经非还原电泳和MALS技术严格确认为1:1异源二聚体。如:经还原及非还原电泳验证,Human CD3E&CD3D 异源二聚体蛋白(Cat. No. CDD-H52Wa)纯度高于95%,经SEC-MALS验证,Human CD3E&CD3D 异源二聚体蛋白(Cat. No. CDD-H52Wa)纯度高于85%。

经ELISA验证在各种应用场景中表现出高活性,并采用多种分析技术进行全面严格质控。如:不同批次的CD3E&CD3D(Cat. No. CDD-H82W6)ELISA验证结果。

经与OKT3、SP34-2、UCHT1等热门抗体的结合验证完全符合药物开发要求,可加速抗体药物的开发进程。如:经ELISA验证,CD3E&CD3D (Cat. No. CDD-H52W1) 可以与BCMA×CD3 双特异性抗体结合,线性区间为0.08-3 ng/mL。 与Human IgG1 Fc Protein, Tag Free (MALS verified)(Cat. No.FCC-H5214) 不结合。

可应用于抗体免疫滴度检测,抗体筛选,亲和力测定,抗体质控和临床血药浓度分析等。如:经SPR验证,BCMA×CD3 双特异性抗体可以与CD3E&CD3D(Cat. No. CDD-H52W1)异源二聚体特异性结合,亲和力常数为31.8 nM,可应用于亲和力测定和抗体药物鉴定。


相关阅读
双抗大有可为:多发性骨髓瘤免疫治疗新突破
GPRC5D,治疗多发性骨髓瘤的下一个热门靶点
点击了解“膜杰作”——多次跨膜靶点蛋白开发技术平台及系列产品



























 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!


























 膜杰作
膜杰作 Star Staining
Star Staining



















 CD3全系列靶点蛋白:CD3E(
CD3全系列靶点蛋白:CD3E( His,His&Avi,Fc,Llama Fc,Flag等多标签设计
His,His&Avi,Fc,Llama Fc,Flag等多标签设计 Human、Mouse、Rat、Rabbit、Cynomolgus等多种属选择
Human、Mouse、Rat、Rabbit、Cynomolgus等多种属选择






