胃癌具有较高的发病率及死亡率。根据国家癌症中心数据,在我国胃癌发病率排第三位。近年来,随着全球老龄化加剧、年轻患者的诊断发病率的不断提升,全球及中国胃癌患者技术预计将持续增长。手术可能是根治胃癌的唯一方法,但仅适合早期患者,进展期患者需要根据胃癌分型和分类对可手术治疗的患者采取手术治疗、联合放化疗、生物靶向药治疗等手段的综合治疗,对不可手术的患者选择靶向药治疗或其他支持治疗,从而达到延长患者生存期、改善生活治疗的目的。(文末附胃癌药物靶点及药物研发进展)
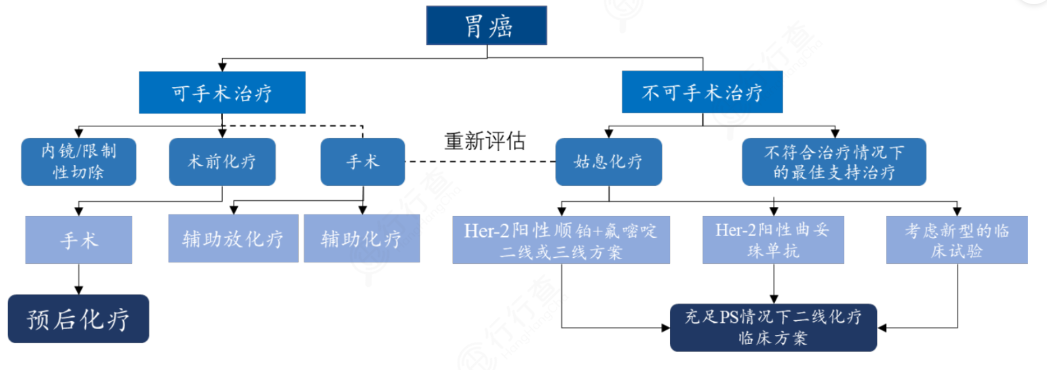
胃癌的系统性治疗方案
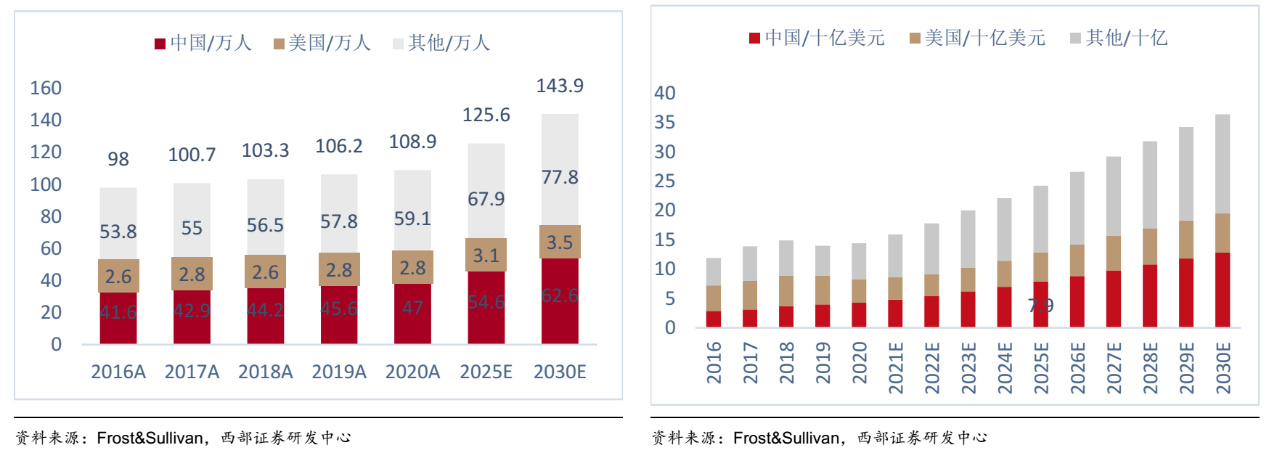
根据Frost&Sullivan报告,2020年,中国胃癌药物市场规模达到43亿美元,预计于2025年将增至79亿美元,复合增长率未12.8%。
胃癌新发病例数及药物市场规模
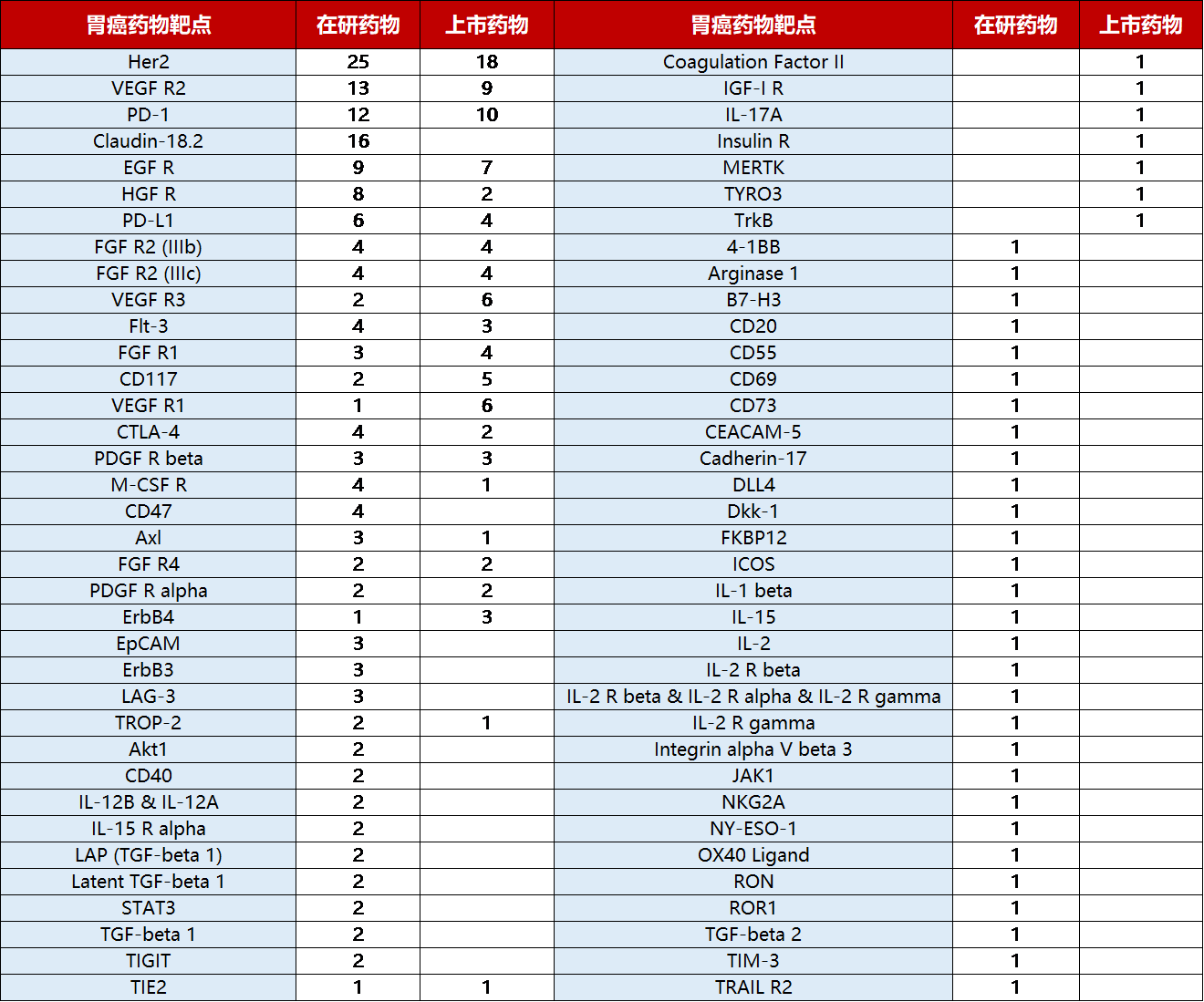
目前,临床上获批用于治疗胃癌的靶向药物主要集中在Her2、VEGFR2、PD-1靶点。而这仍不能完全满足患者的治疗需求,越来越多的新靶点药物进入临床试验,如明星靶点Claudin 18.2,有望为胃癌患者带来新的希望。下面小编为大家梳理一下几个热门的胃癌靶点及代表药物。
Her2是胃癌第一个也是最重要的一个靶点,在胃癌当中的表达率大概是在15%左右。目前,Her2阳性晚期胃癌的一线标准治疗是曲妥珠单抗联合氟尿嘧啶和铂类化疗;二线治疗以紫杉醇/多西他赛/伊立替康化疗为主,疗效欠佳;三线治疗阿帕替尼、纳武利尤单抗的治疗获益十分有限。
Trastuzumab
Trastuzumab(曲妥珠单抗)是第一个经过验证的一线治疗胃癌和胃食管连接部癌的靶向治疗药物。早期胃癌主要通过手术治疗,晚期胃癌患者一线治疗首选曲妥珠单抗(Her2+患者)与以PD-1为基础的联合疗法(Her2-患者),其中Her2-患者化疗的mOS只有12个月左右,PD-1联合治疗的mOS可达到16-21个月。二线及之后获批的药物主要有雷莫芦单抗、抗血管生成抑制剂药物甲磺酸阿帕替尼、PD-(L)1单抗等,二线治疗ORR不足40%,mOS小于1年,三线后的mOS不超过半年。78%的胃癌患者Her2为阴性,缺少有效治疗的靶向药物,总生存期不足一年,存在大量的临床需求缺口。靶向Claudin 18.2等创新靶点药物的开发有望为这些患者带去新的希望。
T-DXd
T-DXd(DS-8201)是全球首个获批治疗Her2阳性晚期胃癌的ADC药物,并已于2022年3月在中国提交上市申请。DESTINY-Gastric01研究显示对于≥3线治疗的Her2阳性晚期胃癌,T-DXd组比单药化疗组的PFS(5.6 vs 3.5个月)和OS(12.5 vs 8.9个月)均显著延长。T-DXd组和化疗组的ORR分别为51.3%和14.3%,DCR分别为85.7%和62.5%,DOR分别为12.5月和3.9个月。
Claudin 18.2 在多个癌组织中的表达呈高度特异性尤其在胃癌和胰腺癌中存在较高的表达。在胃癌或胃食管结合部癌中,高达60%的患者检测到Claudin 18.2的高度表达。目前,已经开发了针对Claudin 18.2进行癌症治疗的多项免疫疗法,包括抗体药、CAR-T 和 ADC 等多种类型,其中最具代表性的为 Zolbetuximab(IMAB362)、CAR-T 制剂 CT041 和 TJ-CD4B。
Zolbetuximab
Zolbetuximab(IMAB362)是一种抗 Claudin 18.2 单克隆抗体,也是目前进展最快的药物。II 期随机临床研究(FAST 研究)对比了 Zolbetuximab 联合 EOX 和单用 EOX 用于 Claudin 18.2 阳性食管、胃/胃食管结合部腺癌一线治疗的有效性与安全性。结果显示:Claudin 18.2表达患者比例≥70%,接受Zolbetuximab+EOX方案治疗的mPFS为9个月,mOS为16.5个月;接受EOX方案治疗的mPFS为5.7个月,mOS为8.9个月。且Zolbetuximab+EOX方案联合治疗总体可耐受,不良事件可控。
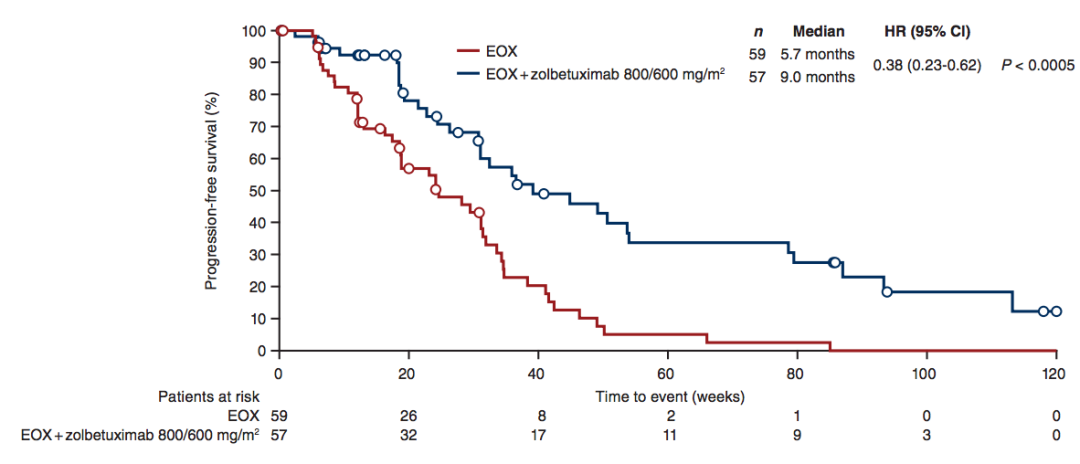
Zolbetuximab 联合 EOX 较单用 EOX 化疗,显著延长 PFS(9.0 个月 vs 5.7 个月)
CT041
CT041是细胞治疗企业科济药业自主研发的国际上首个针对 Claudin 18.2 的自体CAR-T候选产品。2021年欧洲肿瘤内科学会(ESMO)年会上,研究者公布了CT041用于治疗Claudin 18.2 表达阳性的晚期消化道肿瘤的 I 期临床试验 (NCT03874897) 结果,疗效数据非常出色:接受CT041治疗的患者,所有患者的整体缓解率达48.6%,疾病控制率达73%;所有胃癌患者客观缓解率(ORR)为57.1%。对于既往接受至少2线治疗失败的胃癌患者,ORR 仍高达 61.1%(11/18),中位无进展生存期(mPFS)为5.4个月,中位总生存期(mOS)为9.5个月。未观察到免疫效应细胞相关的神经毒性、治疗相关死亡和3级或以上细胞因子释放综合征。
血管生成是癌症的特征之一,胃癌通常表达高水平的血管内皮生长因子(VEGF)并分泌促血管生成细胞因子。然而,抗血管生成治疗在胃癌的临床实践中的结果一直存在差异。
Ramucirumab
抗VEGFR2抗体Ramucirumab在二线治疗中,与安慰剂相比,显示出有限的单一治疗效果(REGARD试验);与单独化疗相比,Ramucirumab与紫杉醇的联合略微提高了总生存率(RAINBOW试验)。因此,Ramucirumab和紫杉醇的联合治疗成为新的治疗标准。目前,一项测试Ramucirumab和tusamitamab–ravtansine组合的研究将进一步评估这种有希望的疗效(NCT05071053)。
ACROBiosystems百普赛斯秉承“从靶点蛋白开始,为更好生物医药”深耕生物医药领域多年,胃癌靶点蛋白一应俱全,助力胃癌靶向治疗药物研发。
以下胃癌治疗靶点蛋白ACROBiosystems百普赛斯均可提供,欢迎添加文末小助手咨询~
胃癌药物靶点及药物研发进展(药渡数据)



























 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!


























 膜杰作
膜杰作 Star Staining
Star Staining