在细胞免疫反应中,T细胞的增殖和活化不仅需要T细胞受体TCR识别APC或肿瘤细胞表面MHC提呈的第一信号,还需要共刺激分子提供的第二信号,B7家族是目前发现的共刺激分子家族之一,通过CD28受体家族与B7配体家族相互作用,激活或抑制T细胞的活化与增殖。
B7家族,属于免疫球蛋白超家族。目前已发现11种B7蛋白,即B7-1、B7-2、B7-H1、B7-DC、B7-H2、B7-H3、B7-H4、B7-H5、BTNL2、B7-H6和B7-H7。B7家族与肿瘤进展关联密切,在肿瘤免疫、自身免疫病和器官移植的临床治疗中发挥着十分重要作用无论是单独治疗还是与其他疗法结合,B7家族一直备受瞩目。下面小编就B7家族中几个重磅分别做介绍。>>>点击查看B7家族蛋白详细信息
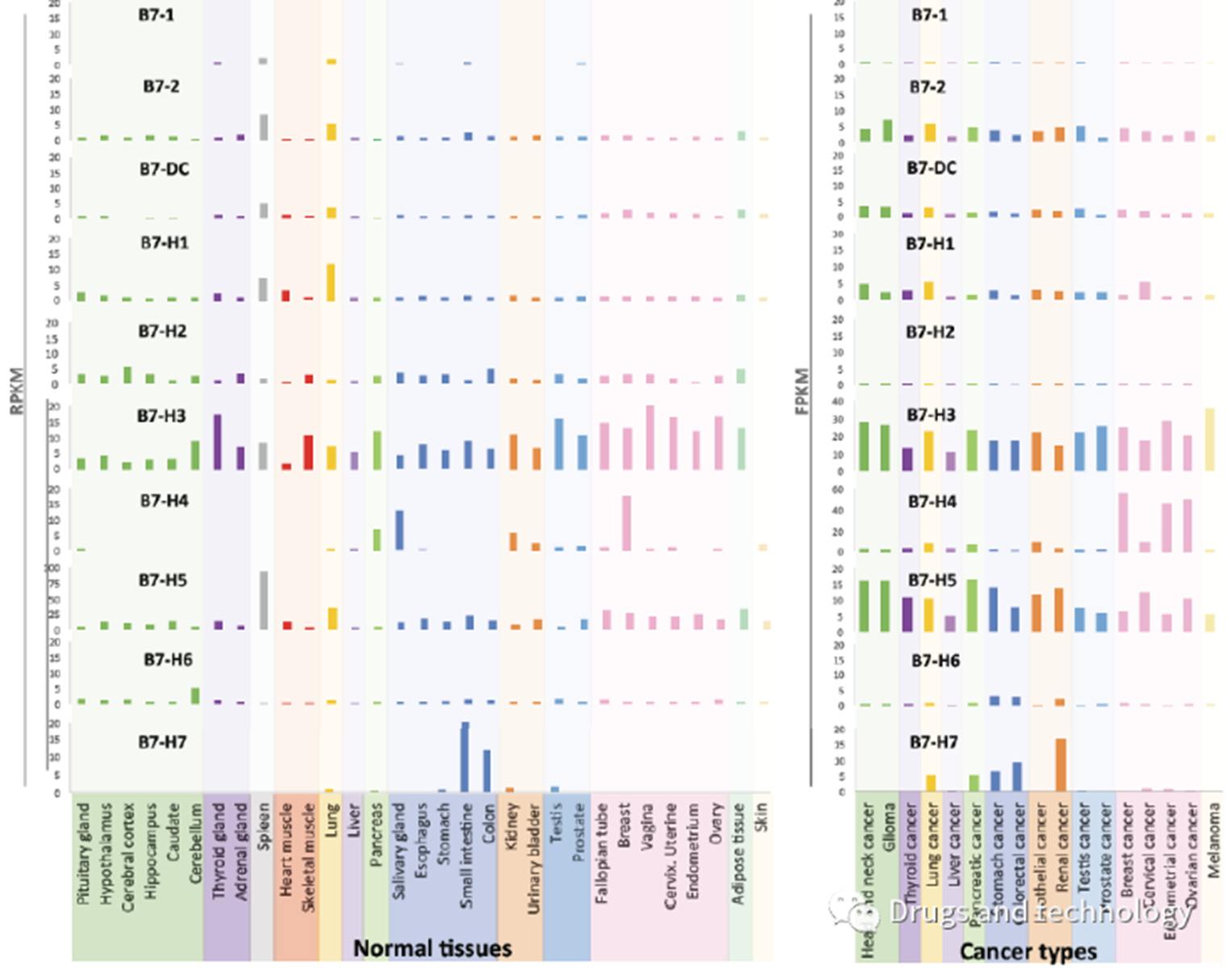
B7家族靶点在正常组织和肿瘤中表达量
B7-H3是一种I型跨膜蛋白,其在免疫系统中具有双重作用。首先,B7-H3作为共刺激因子,对T细胞具有共刺激作用,诱导细胞免疫。其次,B7-H3也具有共抑制作用,使肿瘤逃避免疫反应和抑制NK细胞介导的细胞裂解。
B7-H3在正常组织中很少表达,而在大多数恶性肿瘤中异常表达,帮助肿瘤细胞免疫逃逸,同时赋予肿瘤细胞更具攻击性的表型,因此B7-H3高表达与肿瘤侵袭性和不良预后相关。
目前B7-H3的受体尚未知晓,这使靶向该分子的药物研发面临一定困难。迄今为止尚无FDA批准的针对B7-H3的治疗药物。但已经积极探索了多种靶向B7-H3的药物及疗法,涉及单抗、双抗、ADC以及CAR-T等。吸引国内外诸多药企纷纷布局。而在众多药物中,ADC药物呈现蓬勃发展之势。
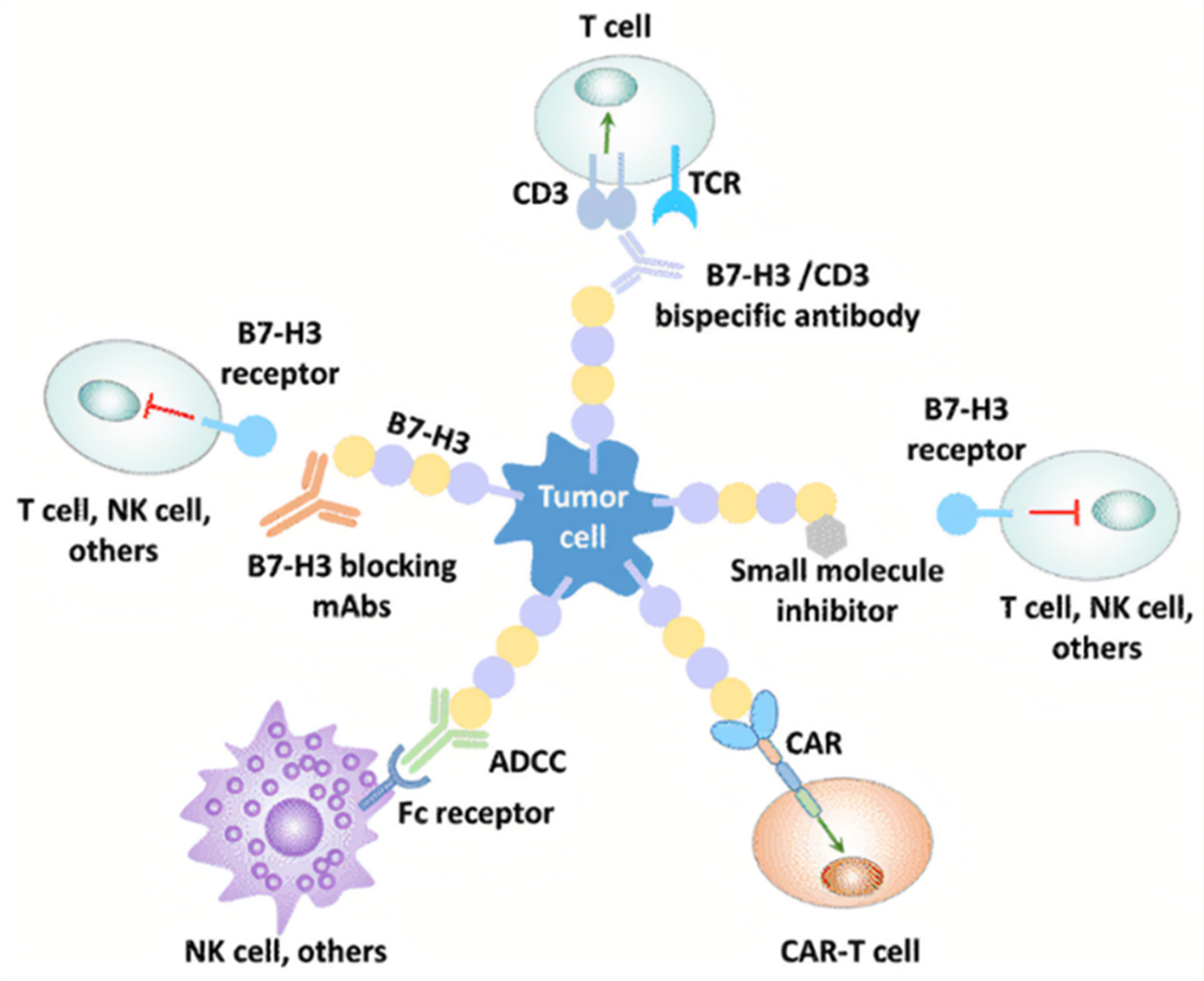
B7-H3的免疫治疗策略
Insight数据库显示,全球进入临床阶段的ADC药物有近10 款,进展最快的是MacroGenics开发的MGC-018,处于II/III期临床阶段;翰森制药HS-20093以及第一三共Lfinatamab deruxtecan(I-DXd; 代号DS-7300)紧随其后,正在开展II期临床试验。国内赛道布局企业还包括百奥泰等。
2023年WCLC 2023报道了I-DXd治疗难治性小细胞肺癌的研究数据,数据显示I-DXd的客观缓解率达52.4%,中位无进展生存期为5.6个月,中位总生存期达12.2个月。但其不良反应导致22.7%的患者终止治疗,有1例患者出现药物相关间质性肺病。
靶向B7-H3的CAR-T疗法也有令人惊喜的进展。9月30日,拓新天成宣布其与美国Tcelltech公司开发的B7-H3 CAR-T细胞疗法TX103的临床试验申请(IND)获得美国FDA批准,用于治疗恶性脑胶质瘤。TX103已于今年6月获得了FDA孤儿药资格,同样用于治疗恶性脑胶质瘤。
相关阅读:B7-H3:突破创新,引领免疫治疗的新时代!
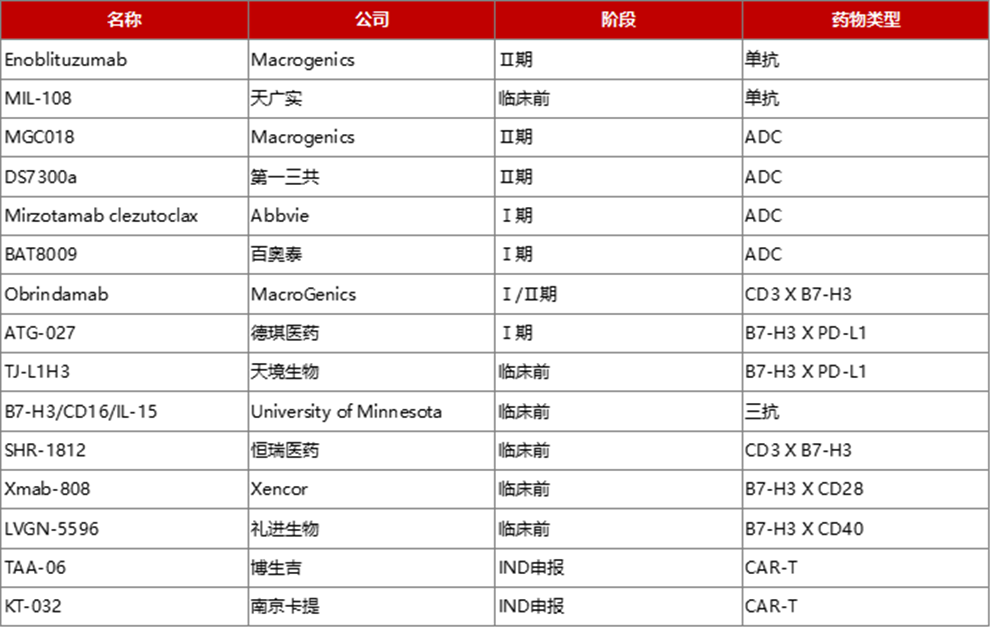
靶向B7-H3的药物研发进展(部分)
B7-H4是B7家族又一重要成员,属于I型跨膜蛋白,由一个信号肽区、一个胞外区、一个跨膜区和一个胞内区组成。B7-H4在正常健康组织中处于相对低的表达水平,在各种癌细胞都过度表达。其表达水平和预后呈负相关。

B7-H4在癌症发生和癌症免疫中发挥重要作用。B7-H4通过调节T细胞功能介导多种免疫抑制机制。研究发现,B7-H4能够阻断效应T细胞的炎症功能,减少IFNγ等细胞因子的产生,并抑制其增殖。此外,B7-H4促进免疫抑制Treg功能,促进IL-10等免疫抑制因子分泌。B7-H4还调节T细胞的分化,抑制其分化为效应T细胞,介导肿瘤的免疫逃逸。
此外,B7-H4还具有其他生物学功能,如预防1型糖尿病(T1D)和胰岛细胞移植。因此,B7-H4已被确定为治疗肿瘤、炎症、自身免疫性疾病等的一个靶点。

B7-H4作用的位置
目前,B7-H4在T细胞表面的受体尚未明确,针对B7-H4的癌症疗法包括单抗、双抗、ADC及细胞疗法,且已在临床前小鼠模型中证明了有效性。在肿瘤治疗中,适应症以乳腺癌和卵巢癌居多。
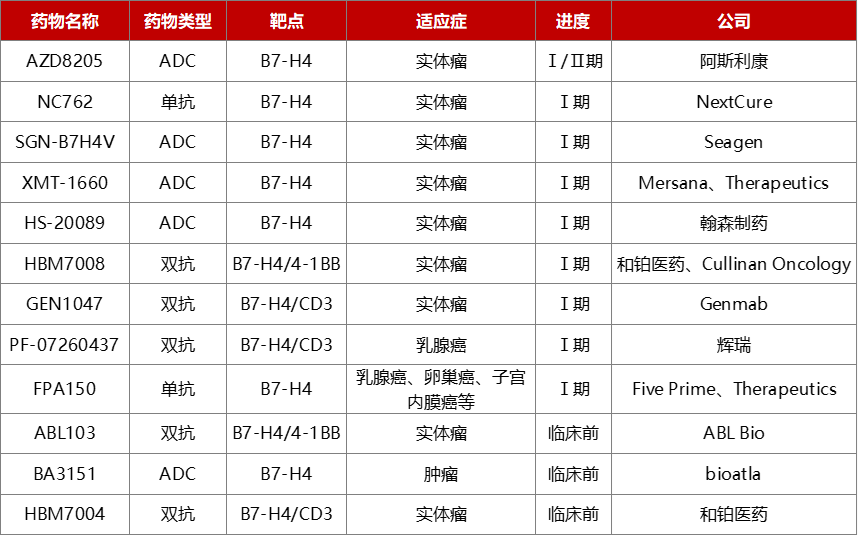
B7H4靶点抗体偶联药物
在靶向B7-H4的药物中,阿斯利康开发的ADC药物AZD8205的进展较快,目前处于1/2期临床。在一项针对26例TNBC(三阴性乳腺癌)患者的临床试验中,采用AZD8205治疗后,总体缓解率高达69%,完全缓解率达36%。AZD8205展示出强大的治疗潜力,可望成为TNBC这种目前仍缺乏有效药物的恶性肿瘤的救命药。

在2023 ESMO大会上,翰森制药将以迷你口头报告的形式公布其B7-H4 ADC药物HS-20089在晚期实体瘤患者中的首次人体/I期试验,领域是转移性乳腺癌,报告编号为381MO。注射用HS-20089是一款由人源化IgG1抗B7-H4单克隆抗体、拓扑异构酶I抑制剂和linker构成的 ADC,具有较高的安全性。
相关阅读:多面B7-H4,潜力不容小觑
B7-H5,又称VISTA,是B7家族一个值得关注的抑制性免疫检查点。在炎症反应中,VISTA通过重编程髓细胞减少TNF-α等促炎细胞因子、增加IL-10等抗炎介质来促进髓细胞免疫抑制功能;通过促进由激活诱导的T细胞死亡来提高外周免疫耐受。
VISTA与其配体的相互作用受pH调节,肿瘤微环境(TME)的酸性pH ~6.0有利于VISTA与p-选择素糖蛋白配体1 (PSGL-1)的结合。靶向肿瘤内pH值可能是一种降低VISTA通路免疫抑制活性和增强抗肿瘤免疫反应的方法。
由于VISTA对维持初始T细胞静息和自身免疫耐受的稳定状态至关重要,可能是癌症免疫治疗以及自身免疫性疾病治疗中一个很有潜力的辅助治疗靶点。

蛋白结构
目前,全球还没有针对VISTA靶点的抑制剂获批上市,但已出现多款在研药物。其中KVA12.1进展较快,已进入2期临床。Curis公司拥有两款VISTA靶向药,即CI-8993和CA-170。
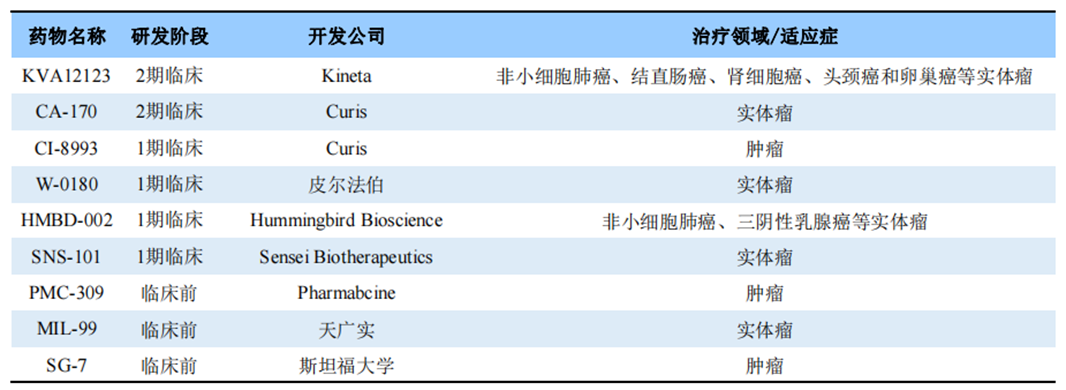
全球部分在研VISTA靶向药(来源:药渡数据)
B7家族对于维持免疫效力和抑制自身免疫的平衡至关重要。B7-H3、B7-H4等成员也已在肿瘤免疫治疗领域大放异彩。
为满足市场需求,ACROBiosystems百普赛斯开发优化了一系列高纯度、天然结构经MALS验证、高生物活性经ELISA/SPR/BLI/Cell based assay等验证的B7家族蛋白,适用于免疫、抗体筛选、细胞活性检测等实验,可加速抗体药物等的开发进程。
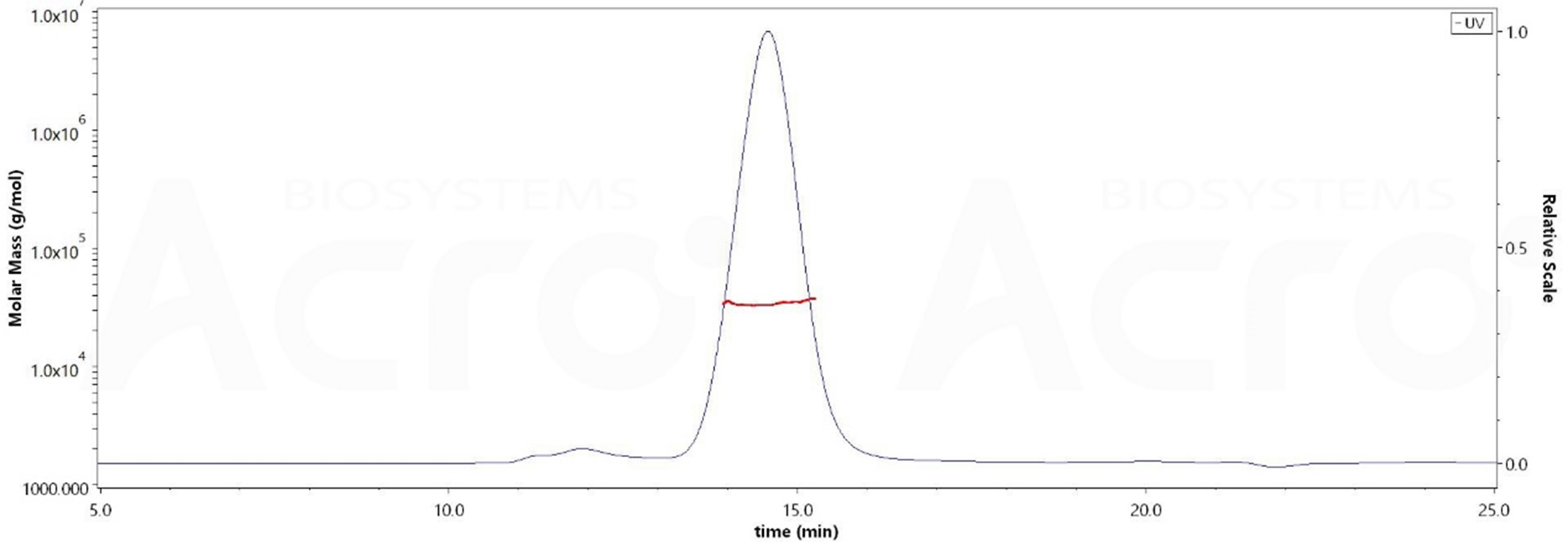
The purity of Human B7-H3, His Tag (Cat. No. B73-H52E2) is more than 90% and the molecular weight of this protein is around 30-40 kDa verified by SEC-MALS.
● 高生物活性经ELISA验证
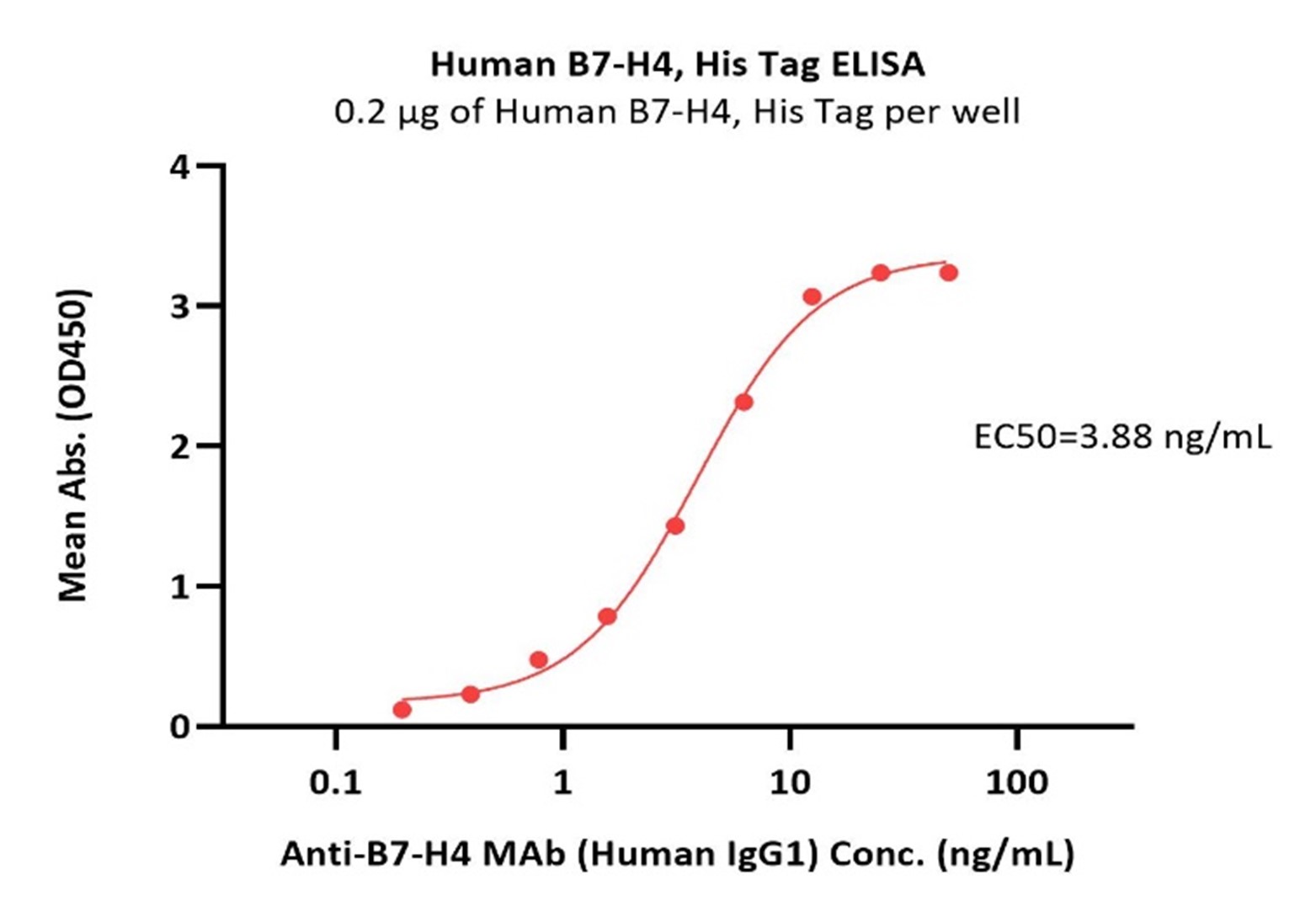
Immobilized Human B7-H4, His Tag (Cat. No. B74-H5222) at 2 μg/mL (100 μL/well) can bind Anti-B7-H4 MAb (Human IgG1) with a linear range of 0.2-6 ng/mL (QC tested).
● 高生物活性经SPR验证
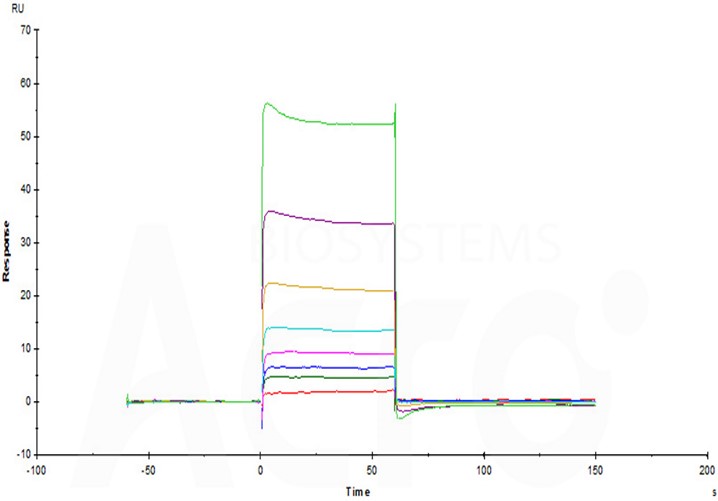
Human VSIG3, Fc Tag (Cat. No. VS3-H5258) captured on CM5 chip via Anti-human IgG Fc antibodies surface can bind Human B7-H5, His Tag (Cat. No. B75-H52H0) with an affinity constant of 53.4 μM as determined in a SPR assay (Biacore T200) (Routinely tested).
● 高生物活性经Cell-based assay验证
Human B7-H3, His Tag (Cat. No. B73-H52E2) inhibits Anti-CD3-induced proliferation of PBMC. The EC50 for this effect is 2.24-3.36 μg/mL (Routinely tested).
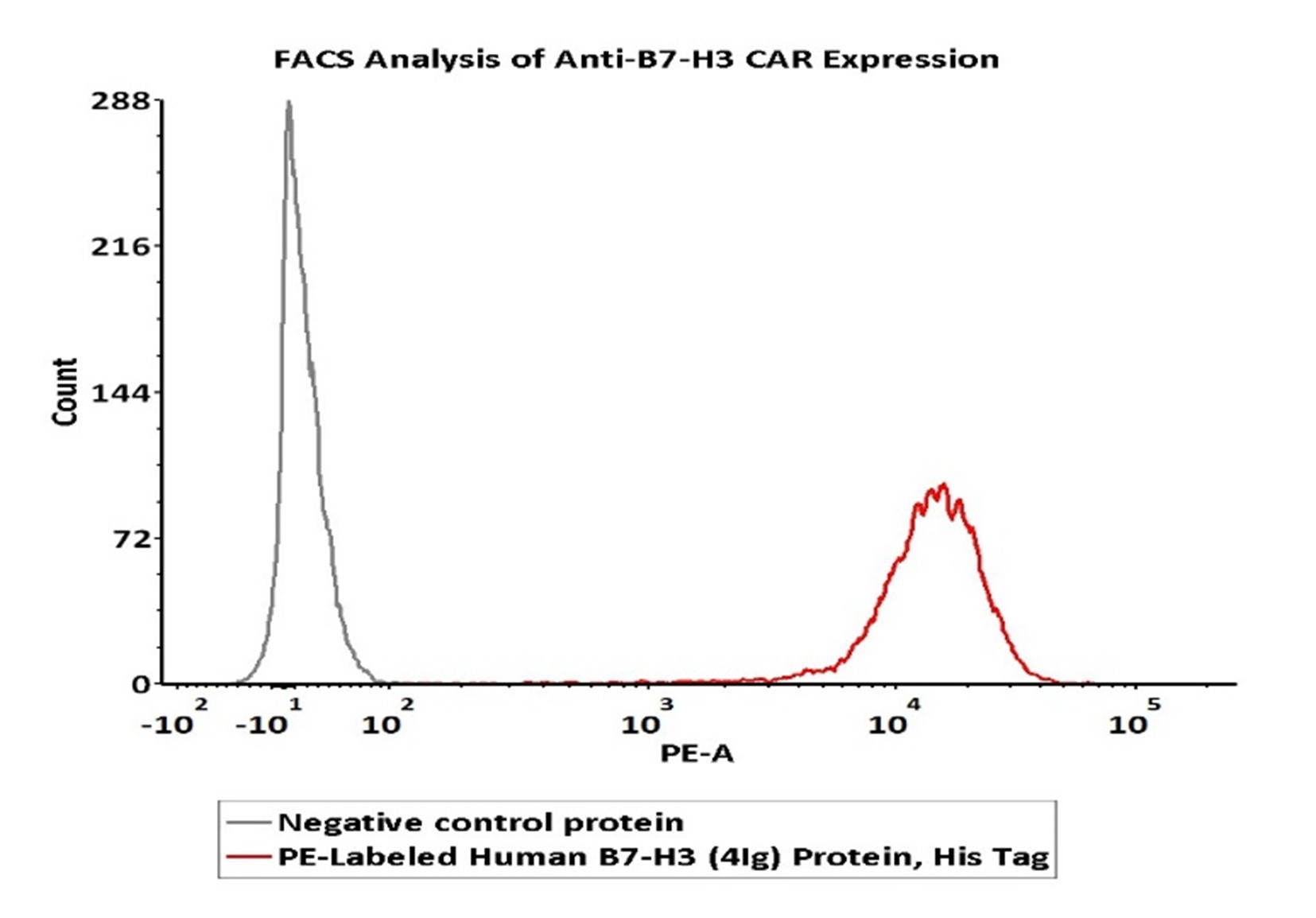
5e5 of anti-B7-H3 CAR-293 cells were stained with 100 μL of 1:50 dilution (2 μL stock solution in 100 μL FACS buffer) of PE-Labeled Human B7-H3 (4Ig), His Tag (Cat. No. B7B-HP2H9) and negative control protein respectively. PE signal was used to evaluate the binding activity (QC tested).
>>>点击查看更多免疫检查点蛋白
>> 更多双抗靶点蛋白及服务
>> 更多ADC靶点蛋白
>> 更多CAR-T热门靶点蛋白




















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!

































 膜杰作
膜杰作 Star Staining
Star Staining