据中国国家流感中心数据显示,2023年4月3日-2023年12月17日(以实验日期统计),A(H1N1)pdm09亚型流感病毒1829株(97.3%)为A/Victoria/4897/2022的类似株;A(H3N2)亚型流感病毒770株(47.3%)为A/Darwin/9/2021(鸡胚株)的类似株;760株(46.7%)为A/Darwin/6/2021(细胞株)的类似株;B(Victoria)系260株(96.7%)为B/Austria/1359417/2021的类似株。2023年第50周第783期中国流感监测周报最新数据显示,全国报告213起流感样病例暴发疫情,最近一周流感病毒毒株以A(H3N2)亚型为主,其次为B(Victoria)系。
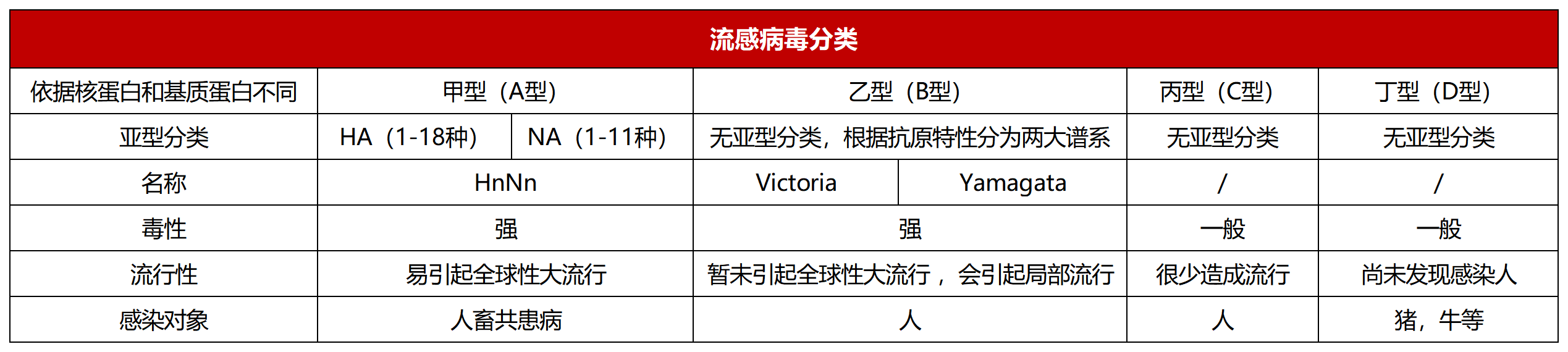
流感病毒属于正粘病毒科的RNA病毒,根据病毒核蛋白和基质蛋白,分为甲、乙、丙、丁(或A、B、C、D)四型(见表1)。甲型流感病毒根据病毒表面的血凝素(HA)和神经氨酸酶(NA)的蛋白结构和基因特性,可分为多种亚型。目前,发现的HA和NA分别有18 个(H1-18)和11个(N1-11)亚型。甲型流感病毒宿主众多,除感染人外,在动物中广泛存在,如禽类、猪、马、海豹以及鲸鱼和水貂等。乙型流感病毒根据HA基因型分为Victoria系和Yamagata系,既往多个流行季在人群中交替流行或混合流行。
流感病毒的分类
“西班牙流感”是人类历史中已知且有翔实记录的最为严重的流感大流行。
首次分离到甲型流感病毒——A(H1N1)亚型。20世纪30年代中期,世界上诞生了第一支用鸡胚生产的灭活甲型流感疫苗。
成功研发了包括A(H1N1)亚型和B 型流感病毒在内的二价灭活流感疫苗。
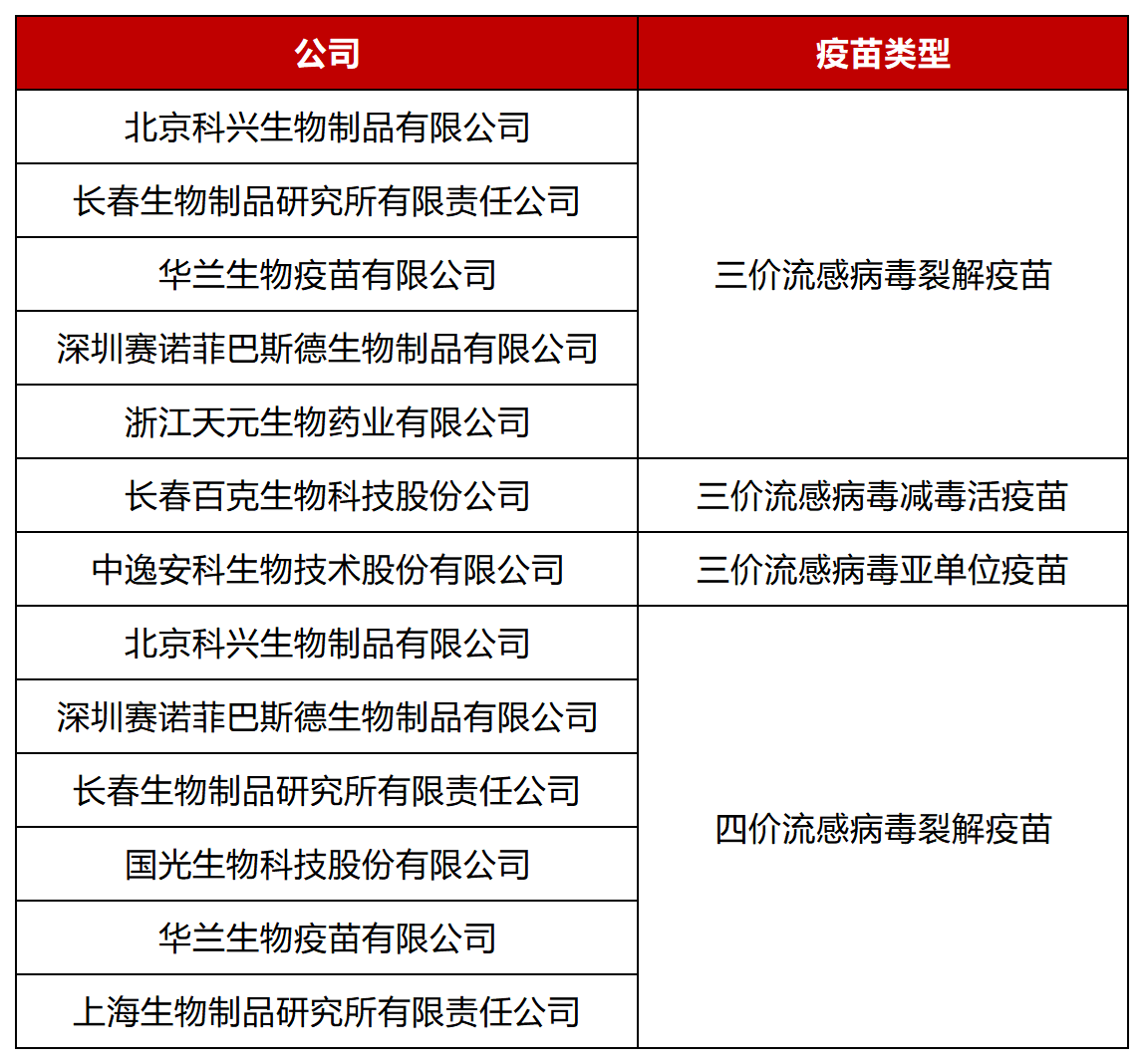
甲型流感病毒H3N2 大流行,提出了三价灭活流感疫苗的需求;同年,裂解疫苗在美国获得授权。英国首先批准了具有高度免疫原性的血凝素(HA)和神经氨酸酶(NA)抗原研制成的亚单位疫苗。佐剂疫苗(铝佐剂和水包油佐剂MF59、AS03)、高剂量疫苗Fluzone 相继开发。美国食品药品监督管理局(FDA)分别批准了四价流感裂解疫苗Fluarix 和重组蛋白三价流感疫苗FluBlock。我国使用的流感疫苗包括三价灭活流感疫苗(IIV3)、四价灭活流感疫苗(IIV4)和三价减毒活疫苗(LAIV3),新一代疫苗研发技术也正逐步被用于流感疫苗的研发,包括病毒样颗粒(VLP)疫苗、多肽疫苗、病毒载体疫苗和核酸疫苗。
接种流感疫苗是预防和控制流感病毒感染及其严重并发症的有效手段,但由于流感病毒抗原的变异性,导致疫苗毒株与当年的流行毒株的抗原性并不完全匹配,造成流感疫苗的有效性降低,不能有效预防季节性和大流行流感,因此研发通用疫苗成为当前的主要趋势。
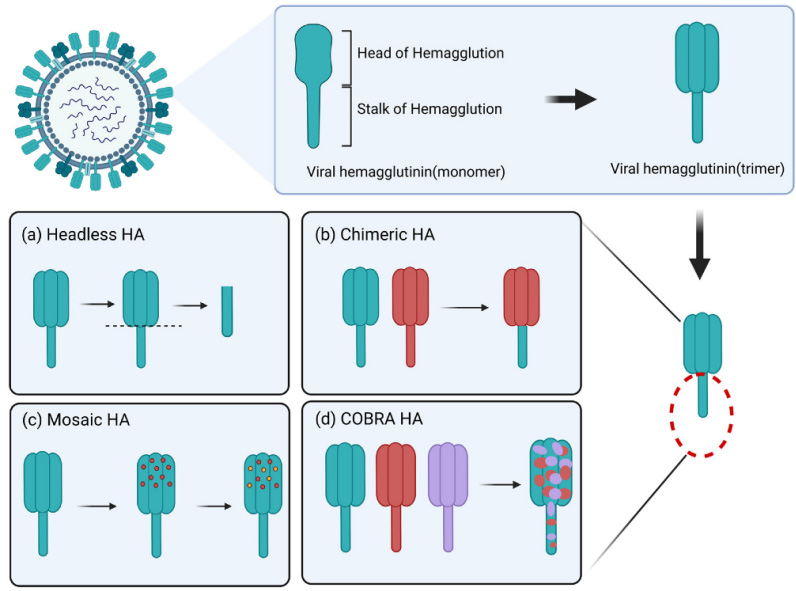
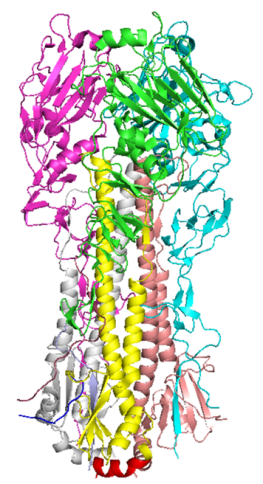
血凝素(HA)介导病毒附着在唾液酸化的宿主细胞受体上,在感染过程中通过与膜的融合进入,其包括球状头部结构域和茎部结构域,HA诱导的特异性抗体具有中和作用。HA的高糖基化降低了对头部结构域的免疫应答,较低的免疫压力使HA茎部结构域与头部结构域相比相对保守。目前基于HA的通用流感疫苗研发策略主要有:保持HA完整结构,但毒株特异性的HA头部使用另一种更为保守的HA头部替换,从而开发出一种新的嵌合HA疫苗;或者去除头部结构,仅保留具有免疫原性的茎部;基于计算优化的广谱反应性抗原的HA 茎部和头部诱导特异性交叉反应抗体等。
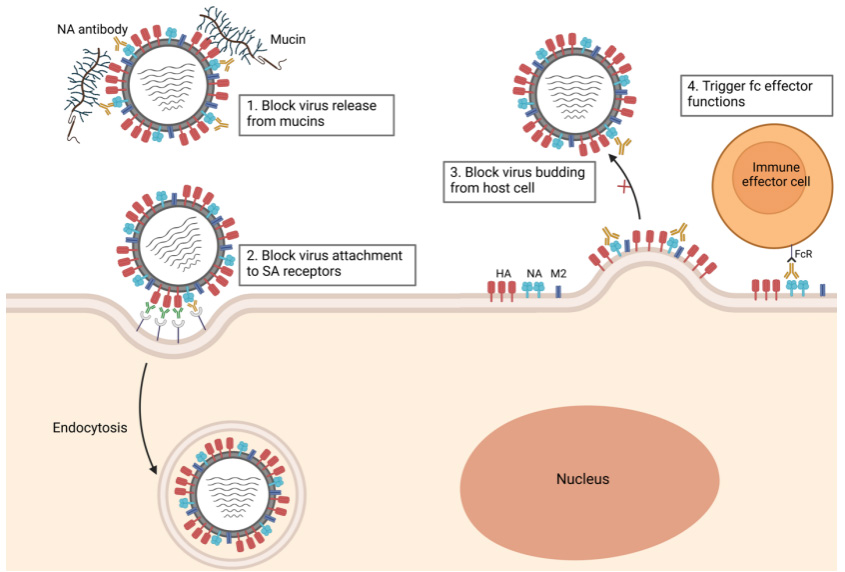
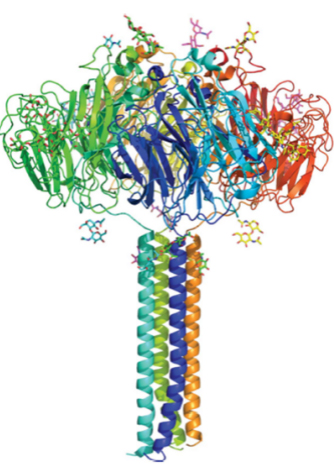
神经氨酸酶(Neuraminidase,NA)NA是流感病毒表面的一种四聚体糖蛋白,主要通过切割宿主细胞膜上的病毒唾液酸受体来促进病毒颗粒的释放并防止后代病毒在细胞表面的积累,从而在病毒传播中起重要作用。抗NA抗体可缩短流感病程并影响病毒传播。位于222~230个氨基酸残基之间的NA酶解位点在甲型和乙型流感病毒中高度保守。针对该表位的单克隆抗体可抑制N1~N9型流感病毒。Skarlupka 等人使用计算优化的广谱反应性抗原方法设计的含有4 种甲型流感病毒NA活性的N1疫苗抗原免疫小鼠,受致死性攻击后小鼠肺病毒滴度低,所有小鼠存活;该疫苗诱导产生的NA抗体能与N1 亚型的禽流感、猪流感和人流感病毒发生交叉反应,并具有中和活性。可见,NA是开发通用流感疫苗极具潜力的靶点。
串联神经氨酸酶(neuraminidase,NA)、HA和M2e
单独使用NA或其保守表位结合HA构建疫苗可产生广泛的IgG抗体反应,但对T细胞反应诱导较差,不足以对异源甲型流感病毒产生保护作用。将NA与HA、M2e蛋白和佐剂结合构建疫苗可产生更好针对同源和异源病毒的保护效果,还能促进Th1/Th2平衡反应的诱导,同时增加对第1组和第2组流感病毒的中和广度。此外,McMahon等和Qiao等模拟并制备了以HA或其茎、NA、M2和NP的通用流感多表位疫苗,发现所有疫苗成分在单剂量给药后都能诱导抗原特异性细胞和体液免疫应答,观察到了显著HA、NA、M2抗体滴度增加和针对NP和M2的强大免疫应答。
为支持流感疫苗的研究开发,ACROBiosystems百普赛斯特开发了流感病毒不同亚型的HA及NA靶点蛋白,可用于各种类型流感疫苗的开发与质量控制阶段,力求加快其研究进程。
◆ 覆盖2023-2024年流行毒株及H5Nx多亚型;
◆ 提供HA天然三聚体构象蛋白及抗体、NA四聚体构象蛋白等疫苗研发所需试剂;
◆ HA及NA全长蛋白及高纯度蛋白可供选择;
◆ His、His & Avi等不同标签可供选择,满足不同实验设计需求;
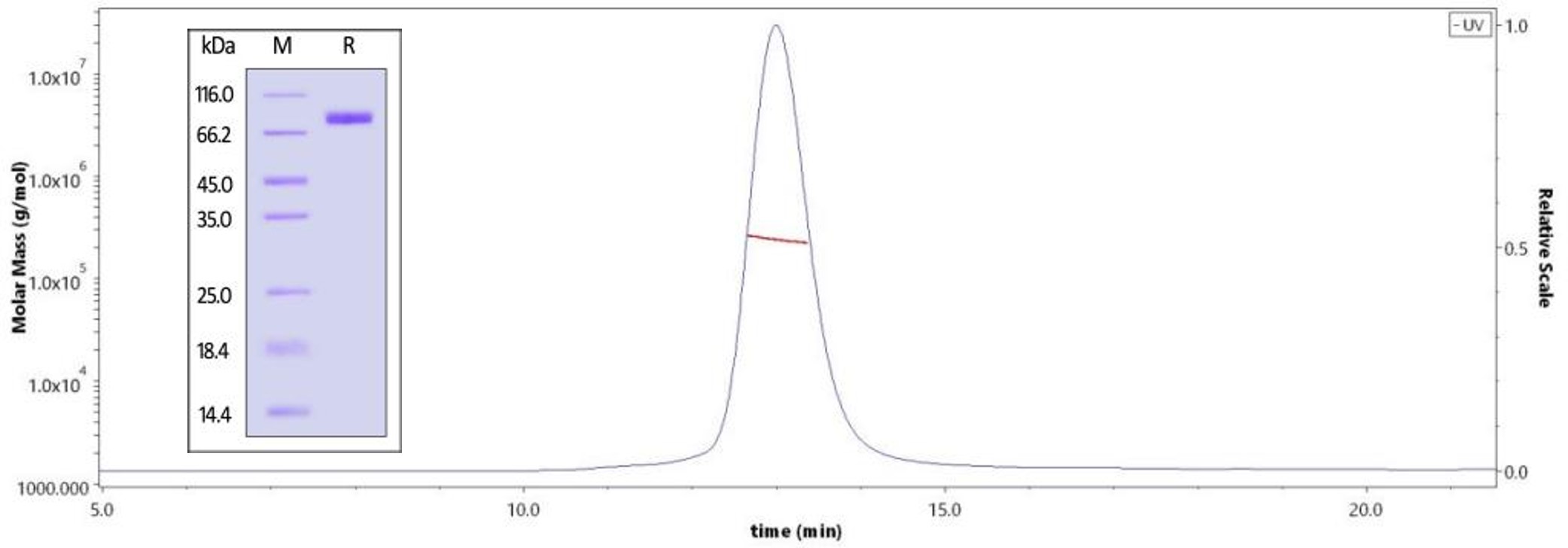
◆ 高纯度经SDS-PAGE及SEC-MALS验证,大于90%;生物活性经抗体结合实验验证。
The purity of Influenza A [A/Darwin/6/2021 (H3N2)] HA Protein, His Tag (Cat. No. HA2-V52H5) is more than 90% and the molecular weight of this protein is around 225-255 kDa verified by SEC-MALS.
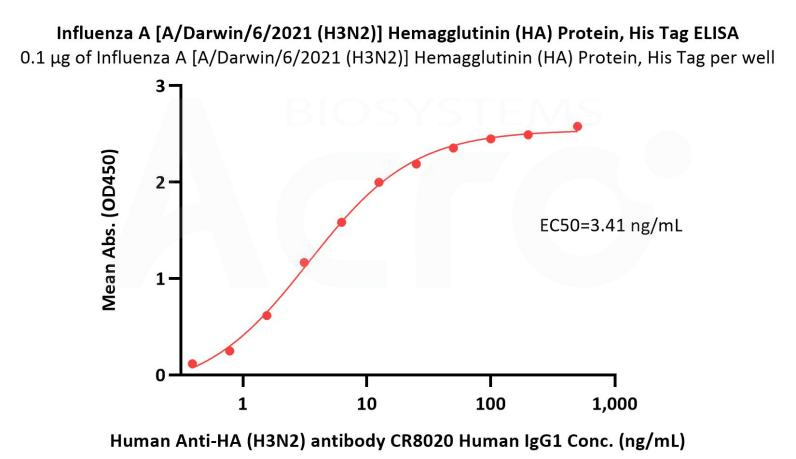
Immobilized Influenza A [A/Darwin/6/2021 (H3N2)] Hemagglutinin (HA) Protein, His Tag (Cat. No. HA2-V52H5) at 1 μg/mL (100 μL/well) can bind Human Anti-HA (H3N2) antibody CR8020 Human IgG1 with a linear range of 0.4-25 ng/mL (QC tested).
参考文献:
1.Li J, Zhang Y, Zhang X, Liu L. Influenza and Universal Vaccine Research in China. Viruses. 2022 Dec 30;15(1):116. doi: 10.3390/v15010116. PMID: 36680158; PMCID: PMC9861666.
2.Piepenbrink M S , Nogales A , Basu M ,et al.Broad and Protective Influenza B Virus Neuraminidase Antibodies in Humans after Vaccination and their Clonal Persistence as Plasma Cells[J].Mbio, 2019, 10(2).DOI:10.1128/mBio.00066-19.




















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!

































 膜杰作
膜杰作 Star Staining
Star Staining