继ADC之后,随着”万物皆可偶联”概念的深入人心,SMDC、PDC、VDC、RDC等创新偶联技术的开发令人眼花缭乱,并取得诸多亮眼成果。其中,放射性核素靶向治疗(RDC)在众多创新技术路线中最为突出,被认为是未来最具潜力的癌症治疗方向之一。
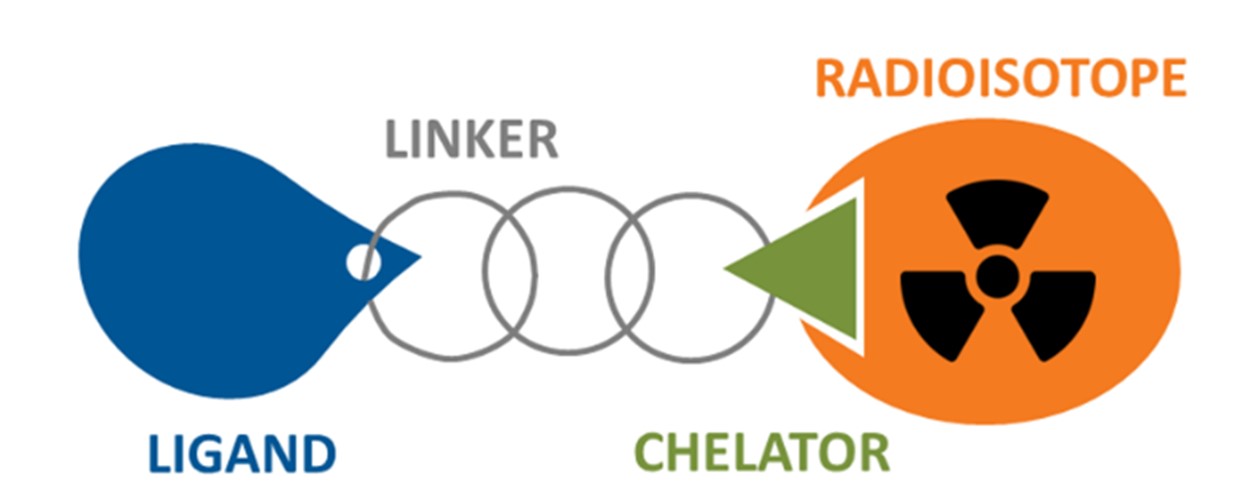
RDC主要由介导靶向定位作用的配体(Ligand)、连接臂(Linker)、螯合物(Chelator)和放射/成像因子(放射性同位素,radioisotope)构成。与传统核药相比,RDC具有更高的靶向性和稳定性,能够在减少对正常细胞的损伤的同时,更有效地杀灭肿瘤细胞。RDC组成与ADC类似,但两者也有诸多区别。
RDC示意图(图片来源:https://www.pharmcube.com/index/news/article/7142)
-
● 配体的精准导向:相较ADC,由于RDC的放射特性,其配体需更精准的导向和更快的代谢率。RDC的配体可以是抗体、多肽和小分子。根据靶向配体的不同,可细分为抗体偶联核素药物(ARC)、小分子偶联核素药物(SMRC)和多肽偶联核素药物(PRC),其中多肽偶联核素药物目前是受到广泛关注的研发方向。由于肿瘤深层位置相较于外围缺少血管,当小分子或者多肽充当RDC的配体时,相对于ADC较小的体积使其更容易进入肿瘤内部组织,发挥杀伤作用。
-
● 药物载荷的差异:RDC与其他偶联药物之间最大的差异是药物载荷。RDC载荷不再是毒性分子,而是放射性核素。使用不同的放射性核素,可以起到显像或治疗的不同功能,部分核素甚至兼备两种能力。
-
● 更高的体内稳定性与安全性:由于放射性核素不需要与细胞直接接触,RDC的Linker在起效过程中无需断裂,使其相对ADC有着更高的体内稳定性与安全性。
-
● 诊疗一体化:RDC是目前唯一能实现诊疗一体化闭环的技术。螯合物具有双重功能,一端可以结合配体,另一端可以与放射性核素形成螯合物。
RDC药物在降低病患死亡风险、延长肿瘤患者生存时间和提高患者生存质量方面效果显著。其独特的结构与理化性质使其成为目前唯一能实现诊疗一体化闭环的技术。其中,Novatis的Pluvicto (lutetium Lu 177 vipivotide tetraxetan)和Locametz是最具代表性的成功案例,它们的成功极大地激发了全球对RDC药物研发的热情,特别是在治疗领域。
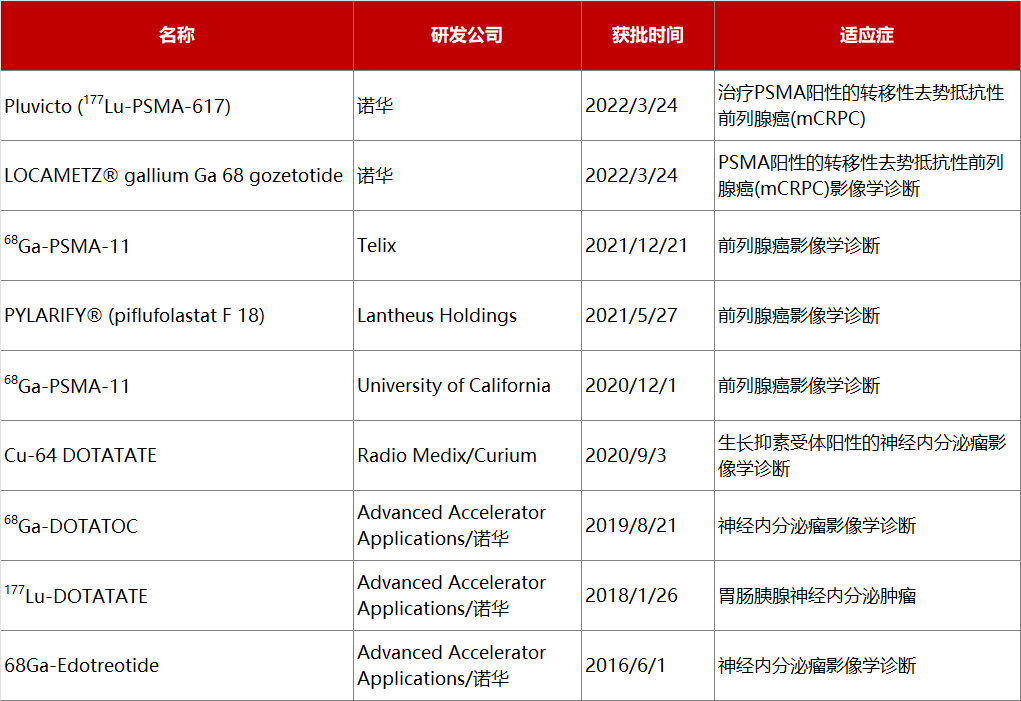
已上市RDC药物(部分)
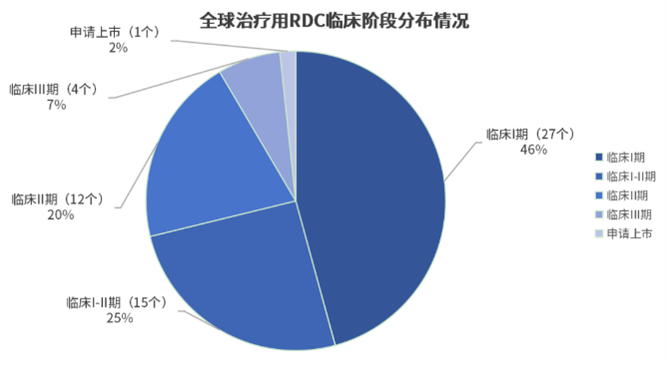
据统计,截至2023年10月,全球已有11款RDC药物获批上市,主要用于治疗前列腺癌和神经内分泌瘤。其中,9款为诊断用药,2款为治疗用药,包括Lutathera和Pluvicto等明星产品。在RDC领域,Novatis公司凭借其卓越的研发实力和市场表现,成为这一赛道的领跑者。
与此同时,包括东诚药业、中国同辐、远大医药、科伦博泰、恒瑞医药等中国的医药企业也在积极布局RDC领域。目前已有超过70条涉及诊断性核药和治疗性核药的在研管线被披露。
在RDC项目的靶点选择上,SSTR/SSTR2和PSMA是布局较多的方向,常用的核素包括177Lu、225Ac、131I、90Y等。
数据来源:药智数据、公开数据整
PSMA作为一种理想的前列腺癌生物标志物,对前列腺癌患者的预后改善具有重要意义。Pluvicto作为首款获得FDA批准用于治疗前列腺特异性膜抗原(PSMA)阳性、既往接受过雄激素受体 (AR)抑制剂和紫杉烷类化疗的转移性去势抵抗性前列腺癌 (mCRPC)成人患者的RDC药物,已经取得了显著的临床效果。随后,由远大医药与Telix合作开发的TLX591(Lu-177 rosopatamab tetraxetan)也进入了III期临床试验,成为另一款备受期待的PSMA靶向RDC药物。目前,全球已有5款靶向PSMA的RDC药物上市,国内也有8款在研产品,远大、东诚、高科的PSMA诊断产品已进入III期临床。PSMA在胃癌等其他实体瘤中也有表达,这意味着未来RDC药物有望拓展更多的适应症。
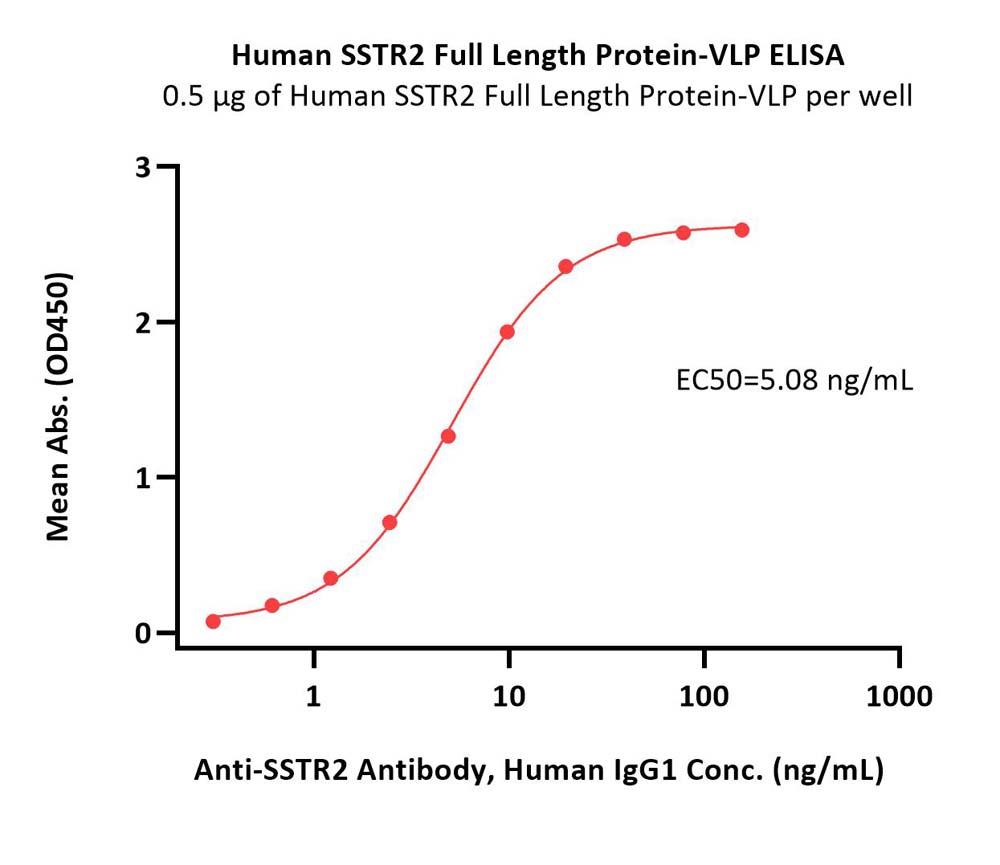
除了PSMA外,SSTR也是RDC药物的重要靶点。生长抑素受体(SSTR)是神经内分泌肿瘤诊疗重要靶点。其中SSTR2在90%的神经内分泌肿瘤中高表达,是神经内分泌肿瘤靶向治疗极具实力的靶点。目前,全球已有包括Lutathera®在内的4款针对SSTR的RDC药物上市,另有6款在研产品。中国的先通医药研发的国内首个SSTR靶点核药镥[177Lu]氧奥曲肽注射液已进入III期临床试验,展示了中国企业在RDC领域的创新能力。此外,原子高科、恒瑞、ITM&远大医药也有相关产品进入Ⅲ期临床。
此外,氟代脱氧葡萄糖(FDG)作为一种重要的显影剂,在癌症临床医学影像和癌症早筛等领域发挥着重要作用18F-FDG全球已有超过47家公司的产品获批上市。此外,FDG还可以用于其他非肿瘤疾病的诊断,如心脏疾病和炎症状态。
同时,Ⅱ型跨膜丝氨酸蛋白酶FAP作为另一个备受关注的靶点,在胃癌、食管癌、肺癌等多种上皮肿瘤中高表达,具有广阔的治疗前景。国内已有企业布局FAP靶点的RDC药物研发,并取得了一定的进展。国内蓝纳成的177Lu-LNC1004注射液已率先进入Ⅰ期临床,北京先通紧随其后布局一对诊疗产品进入I期临床,业界对FAP予以很高的期待。
总体来看相较于PD-1、ADC等已经愈发拥挤与同质化的领域,RDC凭借其独特的诊疗一体化闭环技术和广阔的应用前景,RDC药物的崛起为肿瘤治疗领域带来了新的机遇和挑战。
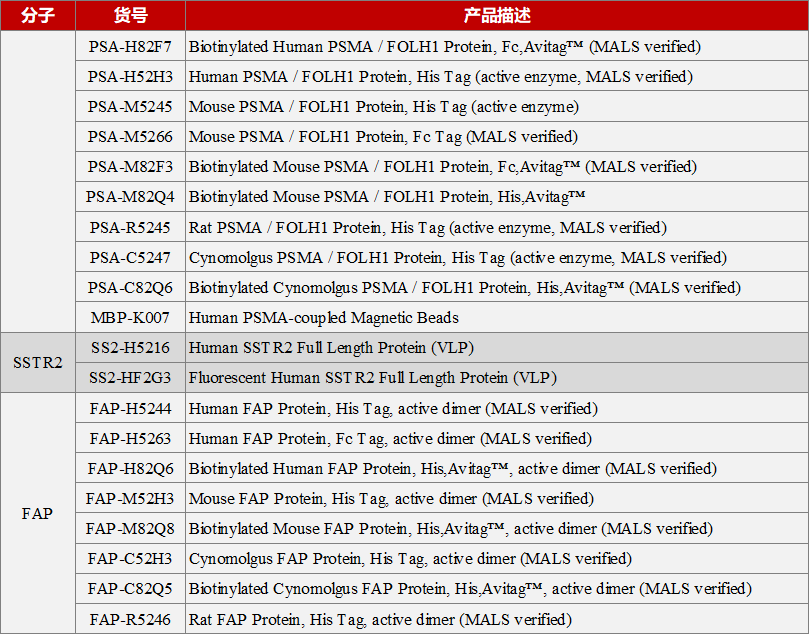
ACROBiosystems百普赛开发了一系列高质量PSMA、SSTR2、FAP蛋白,蛋白均一结构及高纯度经SEC-MALS验证,高生物活性经ELISA/SPR/BLI/FACS验证,高批间一致性且免费提供Protocol,助力相关药物研发进程。
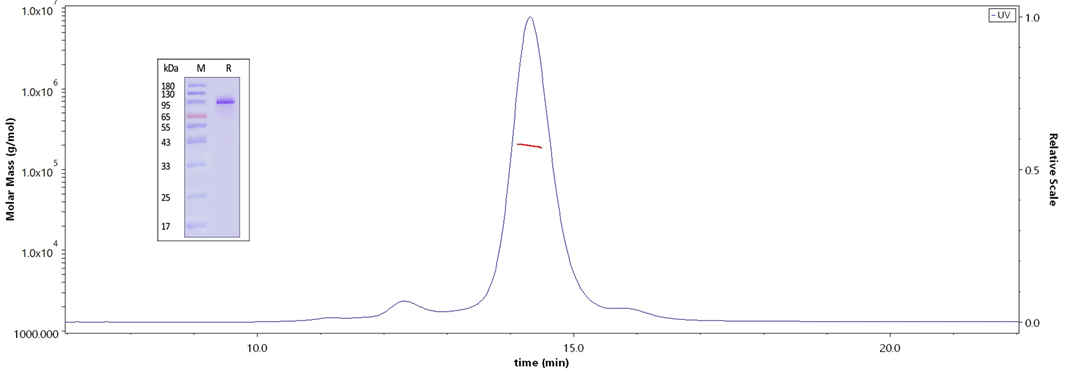
The purity of Biotinylated Cynomolgus PSMA Protein, His,Avitag (Cat. No. PSA-C82Q6) is more than 90% and the molecular weight of this protein is around 180-210 kDa verified by SEC-MALS.
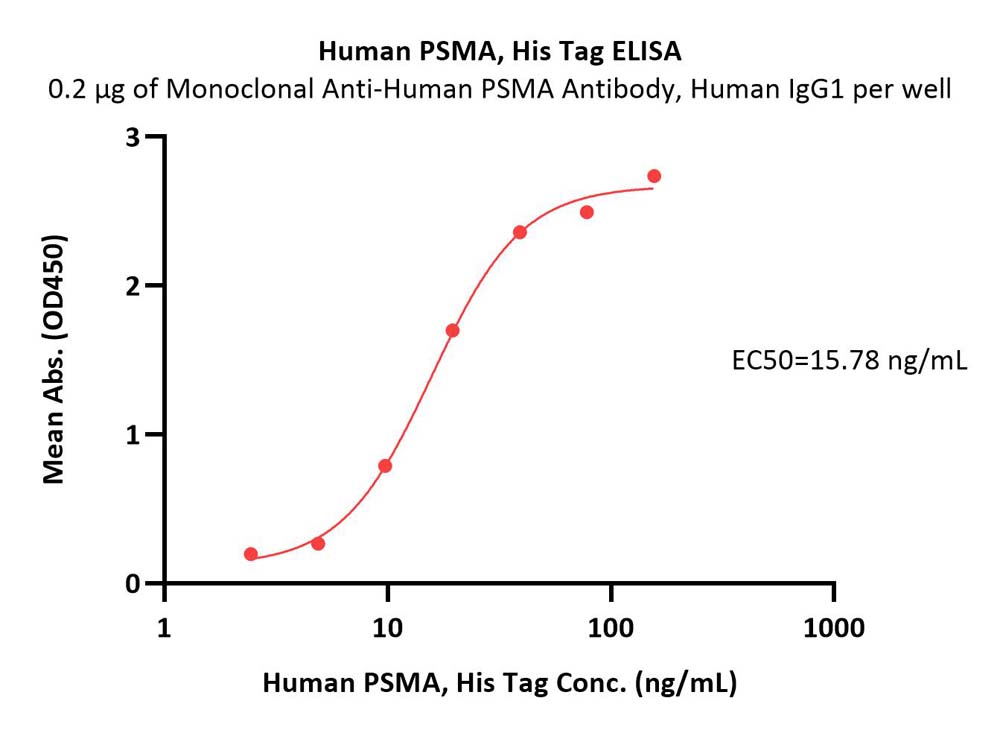
Immobilized Monoclonal Anti-Human PSMA Antibody, Human IgG1 at 2 μg/mL (100 μL/well) can bind Human PSMA, His Tag (Cat. No. PSA-H52H3) with a linear range of 2-39 ng/mL (QC tested).



























 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!


























 膜杰作
膜杰作 Star Staining
Star Staining