5月31日,康方生物发布了全球首创双特异性抗体依沃西单抗(PD-1/VEGF双抗)单药对比帕博利珠单抗一线治疗PD-L1表达阳性(PD-L1 TPS≥1%)的局部晚期或转移性非小细胞肺癌(NSCLC)的III期临床研究的重磅成果,分析显示强阳性结果:达到无进展生存期(PFS)的主要研究终点,成为全球首个且唯一在III期单药头对头临床研究中证明疗效显著优于帕博利珠单抗的药物,证明了其在全球范围内的临床价值和商业化潜力。
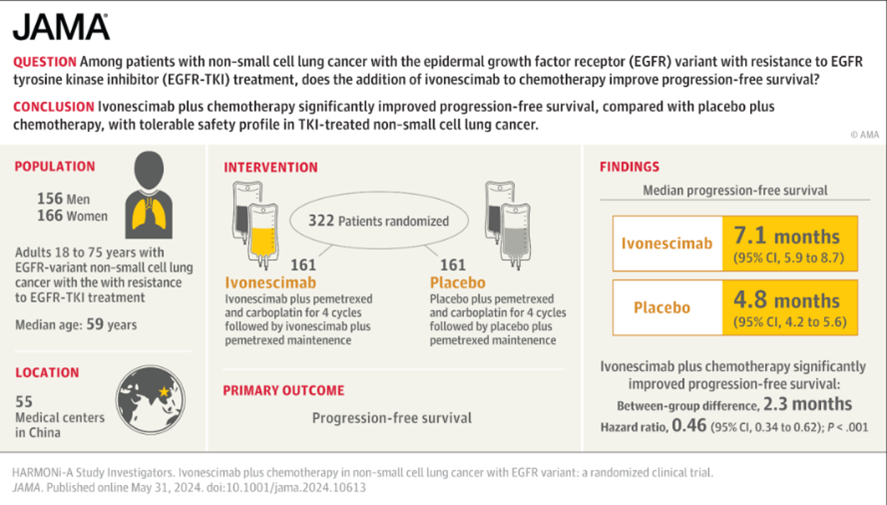
此外,本次ASCO大会中,康方生物以口头报告的形式公布了依沃西HARMONi-A研究的相关数据。HARMONi-A是一项关于依沃西单抗联合化疗用于治疗经EGFR-TKIs治疗进展的EGFR NSQ-NSCLC的随机、双盲、多中心、III期试验,旨在评估和比较依沃西单抗联合化疗与单独化疗在该人群中的有效性和安全性。结果显示研究达到了PFS主要临床终点。
泽璟制药开发的ZG005是一种重组人源化抗PD-1/TIGIT双特异性抗体,它可以通过有效阻断PD-1与其配体PD-L1的信号通路,促进T细胞的活化和增殖;同时,它还可以有效阻断TIGIT与其配体PVR等的信号通路,促使PVR结合CD226产生共刺激激活信号,进而促进T细胞和NK细胞的活化和增殖。这种双重阻断作用使得ZG005在抗肿瘤方面具有协同增强的效果。
据公开资料显示,ZG005是全球率先进入临床研究的同靶点药物之一,目前全球范围内尚未有同类机制药物获批上市。ZG005的I期剂量爬坡研究已经完成,结果显示出良好的安全性。在今年的ASCO会议上也披露了ZG005的Ia期临床的部分结,展现了良好的抗肿瘤效果。
卡度尼利单抗:PD-1/CTLA-4双抗的创新应用
康方生物自主研发的PD-1/CTLA-4双特异性抗体卡度尼利(AK104)为全球首款获批的PD-1/CTLA-4双抗。该药物在安全性、稳定性和抗肿瘤活性等方面均表现出色,尤其在晚期宫颈癌治疗中展现出了显著疗效。此前的临床研究显示,卡度尼利在总体安全性上明显优于已上市的CTLA-4抑制剂,与已上市的 PD-1/PD-L1抑制剂相当。该药于2022年6月获中国药监局批准上市,用于治疗既往接受过含铂化疗治疗失败的复发或转移性宫颈癌患者。目前,康方生物正在通过卡度尼利联合疗法扩展适应症,为更多癌症患者带来希望。
卡度尼利单抗采用了IgG-ScFv结构,可快速介导独立的PD-1或CTLA-4内吞。此外,卡度尼利单抗的 IgG1骨架显示了更稳定的结构特征,且通过Fc段点突变消除了ADCC/ADCP效应的同时减少了免疫相关不良反应的风险。此外,卡度尼利单抗的稳定性是天然IgG4的100倍以上,且不与其他IgG结合,为疗效发挥提供了有力保障。
LBL-024:PD-L1/4-1BB双抗的强效免疫作用
维立志博的双抗LBL-024(PD-L1/4-1BB)以口头报告的形式登上今年ASCO大会。大会上公布了LBL-024单药治疗晚期恶性肿瘤和神经内分泌癌安全性和有效性的首次人体、开放标签、多中心、剂量递增/扩展Ⅰ/Ⅱ期临床研究成果。研究表明,LBL-024对晚期恶性肿瘤患者,特别是接受至少一线化疗失败的肺外神经内分泌癌(EP-NEC)患者,显示出良好的安全性和强有力的有效信号。
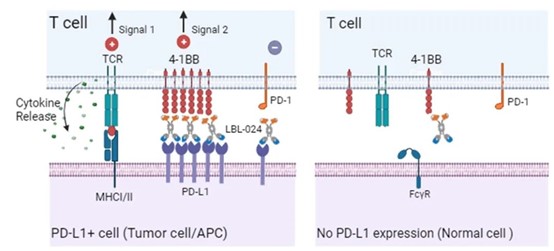
LBL-024能以高亲和力结合PD-L1,阻断PD-L1/PD-1免疫抑制通路的同时,在肿瘤微环境中条件型激活4-1BB共刺激通路,进而激活T细胞发挥强效的免疫作用,产生比抗PD-1/PD-L1单抗更强的抗肿瘤效应。此前,LBL-024已获得国家药品监督管理局药品审评中心(CDE)批准开展一项关键性临床II研究,该项研究将支持其未来上市申报。
LBL-024主要作用机制(图片来源:维立志博官网)
恒瑞医药SHR-1701:PD-L1/TGF-βRII双抗
近日,恒瑞医药宣布其自主研发的PD-L1/TGF-βRII双抗SHR-1701联合或不联合化疗新辅助治疗不可切除的Ⅲ期非小细胞肺癌的概念验证2期临床研究(TRAILBLAZE研究)成果,正式全文在线发表于国际权威学术期刊Cancer Cell。
研究结果显示,在接受新辅助联合治疗的主要队列患者(n=97)中,两项主要终点均达到,诱导后的ORR为58%,18个月EFS为56.6%。




















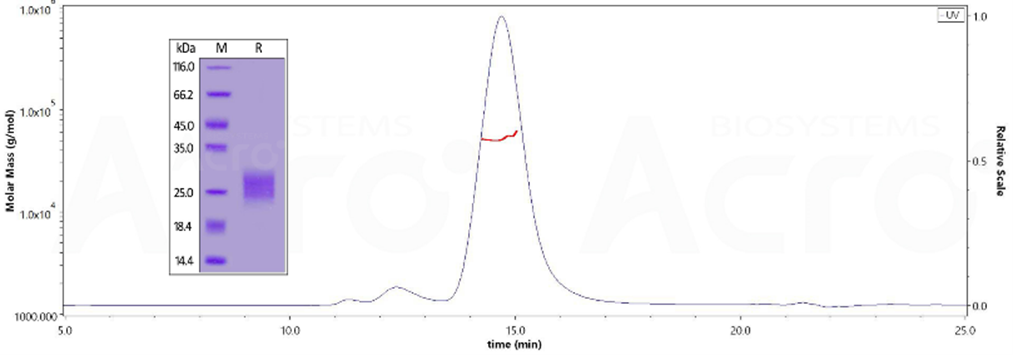
 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!

































 膜杰作
膜杰作 Star Staining
Star Staining