近年来抗体药发展迅猛,在自身免疫类领域的治疗中占据重要位置,抗体药的主要类型为IgG类,其中FcRn凭借其介导的IgG再循环机制,成为开发治疗自身免疫性疾病药物的热门靶点。2021年12月,全球首款FcRn拮抗剂Efgartigimod获美国FDA批准,用于治疗乙酰胆碱受体(AChR)抗体阳性的成人全身型重症肌无力(gMG);2023年6月27日,优时比(UCB)宣布,美国FDA已批准该公司皮下注射靶向FcRn单抗Rozanolixizumab上市,用于治疗抗乙酰胆碱受体(AChR)或抗肌肉特异性酪氨酸激酶(MuSK)抗体阳性成人全身型重症肌无力(gMG);此外Batoclimab也正在申请上市。
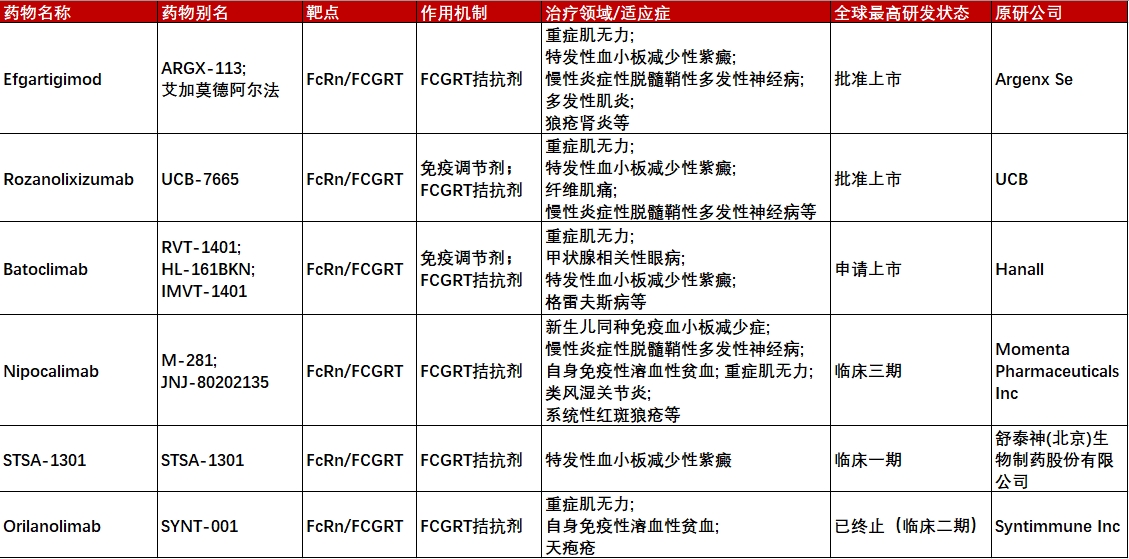
靶向FcRn的药物研发进展一览表
数据来源:药渡
降低内源性IgG的关键:与FnRn亲和力更强的药物设计
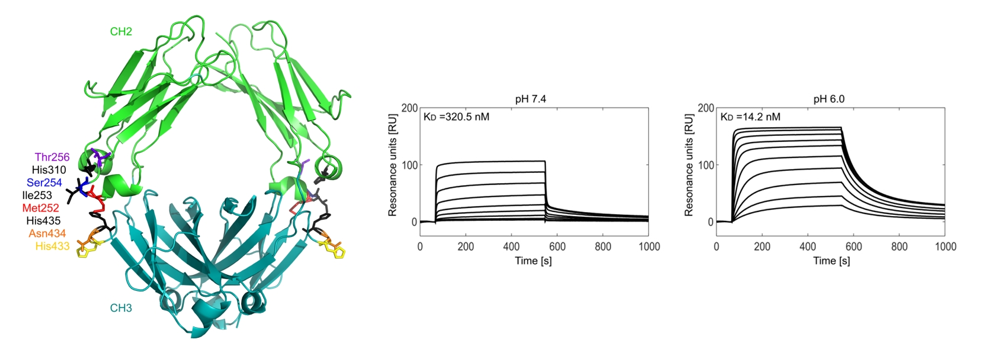
font-style: italic;Efgartigimod中的突变氨基酸及Efgartigimod与FcRn亲和力分析
一项62名健康志愿者的人体研究证实,Efgartigimod具有特异性和快速降低IgG水平的作用。多剂量给药后,受试者血清IgG平均下降约75%,部分个体下降高达85%。所有服用10
mg/kg及以上剂量的受试者均观察到明显的IgG减少,且受试者之间的相对IgG降低幅度一致,进一步证实了Efgartigimod的高效IgG降低能力。
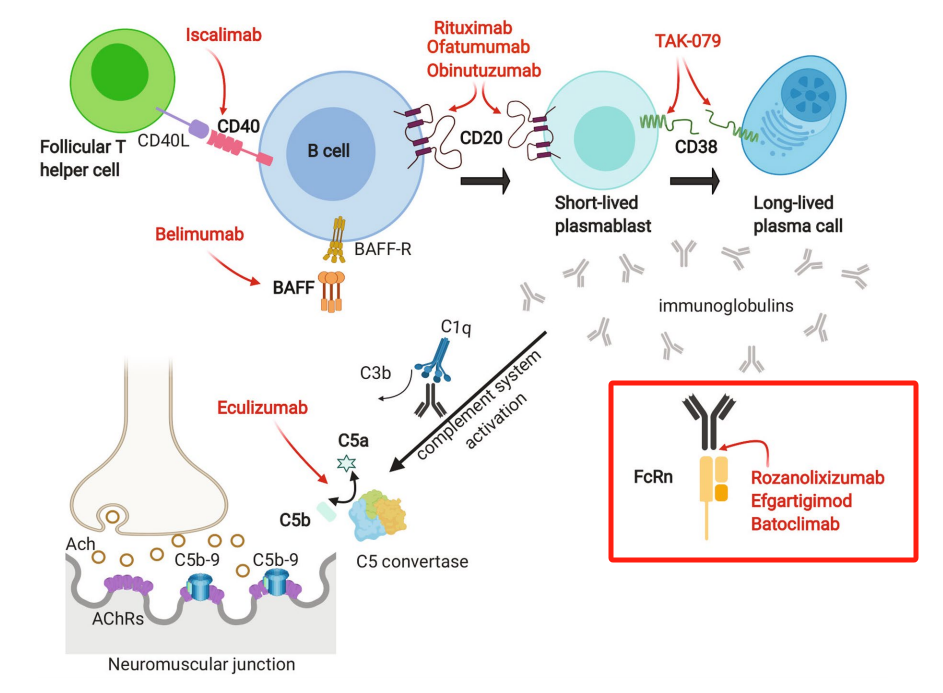
重症肌无力病理生理及治疗性靶点
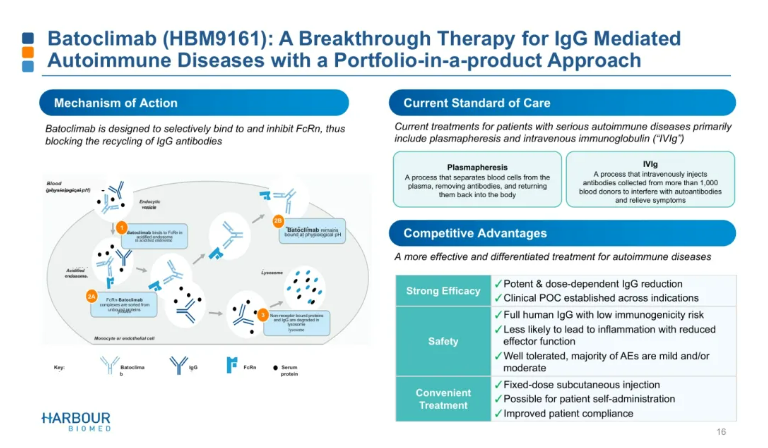
Batoclimab的作用机制
针对自免疫疾病如重症肌无力的新兴治疗方案中,多以IgG类抗体为基础,靶向FcRn的药物作用机制主要在于提高药物与FcRn的亲和力,以促进体内致病性IgG的清除。ACROBiosystems百普赛斯提供高纯度、高稳定性及正确构象的FcRn蛋白,适用于高通量筛选的Human
FcRn结合检测试剂盒,作为同型对照的重组IgG Fc蛋白,全面支持靶向FcRn的创新药物开发。

产品优势
-
HEK293细胞表达:实现翻译后修饰及蛋白正确折叠;
-
高纯度:SDS-PAGE验证纯度>95%,SEC-MALS验证纯度>90%;
-
高稳定性:严格质控为高批间一致性保驾护航;
-
亲和力经SPR&BLI验证,活性有保障,免费提供protocol;
-
提供采用Avitag™定点标记的生物素化FcRn蛋白,标记效率高且标记位点专一明确,方便药物开发及工艺优化过程中基于与链霉亲和素结合的ELISA/SPR/BLI检测;
-
多种属:Human,Mouse,Cynomolgus / Rhesus macaque,Rat,Porcine,Rabbit ,Feline ,Bovine,可全面应用于不同种属交叉实验;
-
低内毒素:<1.0 EU/μg。
应用数据展示
亲和力经抗体结合验证
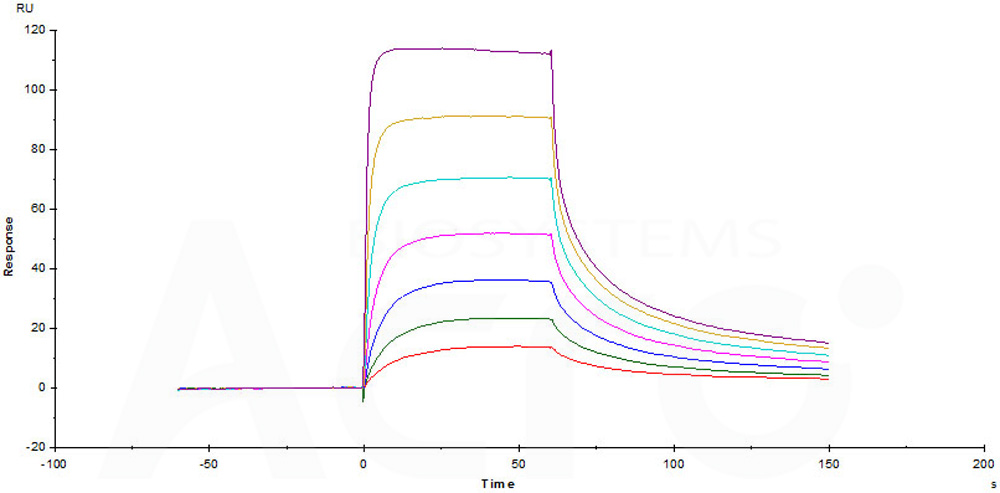
Immobilized Human FCGRT&B2M Heterodimer Protein, His Tag&Strep II Tag (Cat. No. FCM-H5286)
on CM5 Chip via Anti-His antibody, can bind Herceptin with an affinity
constant of 0.261 μM as determined in a SPR assay (Biacore T200) (QC
tested).
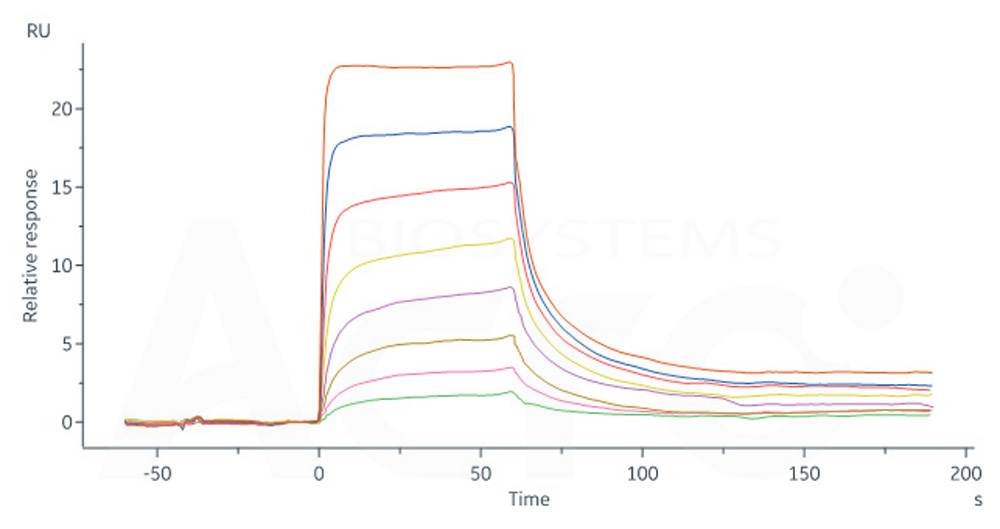
Human FCGRT&B2M Heterodimer Protein, His Tag (Cat. No. FCN-H52W7) captured on CM5 Chip via anti-His antibody can bind Human IgG4 Fc, Tag Free (SPR verified) (Cat. No. IG4-H5205) with an affinity constant of 0.715 μM as determined in SPR assay (Biacore 8K) (Routinely tested).
基于TR-FRET技术和IgG抗体竞争性结合FcRn的机制,ACROBiosystems百普赛斯成功开发出重磅新品:Human FcRn Binding Kit (Cat. No. FRT-01) ,操作简便,结果准确。
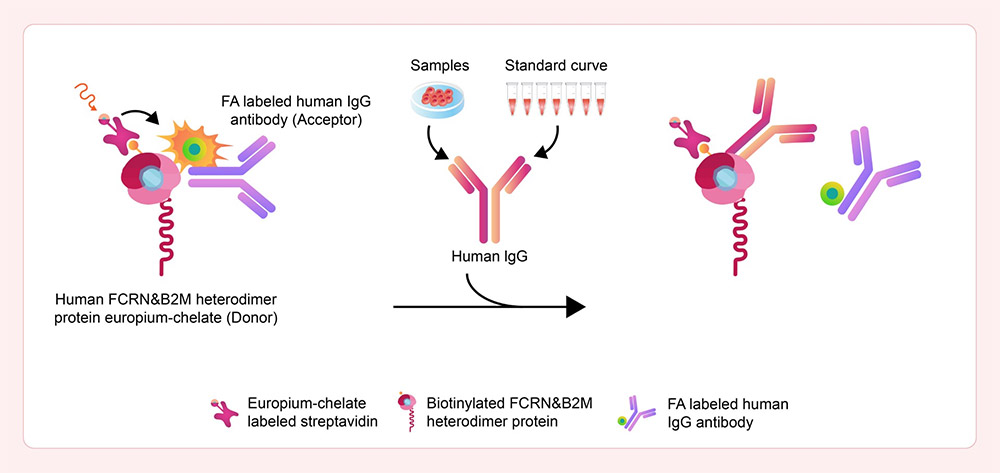
TR-FRET技术检测原理示意图
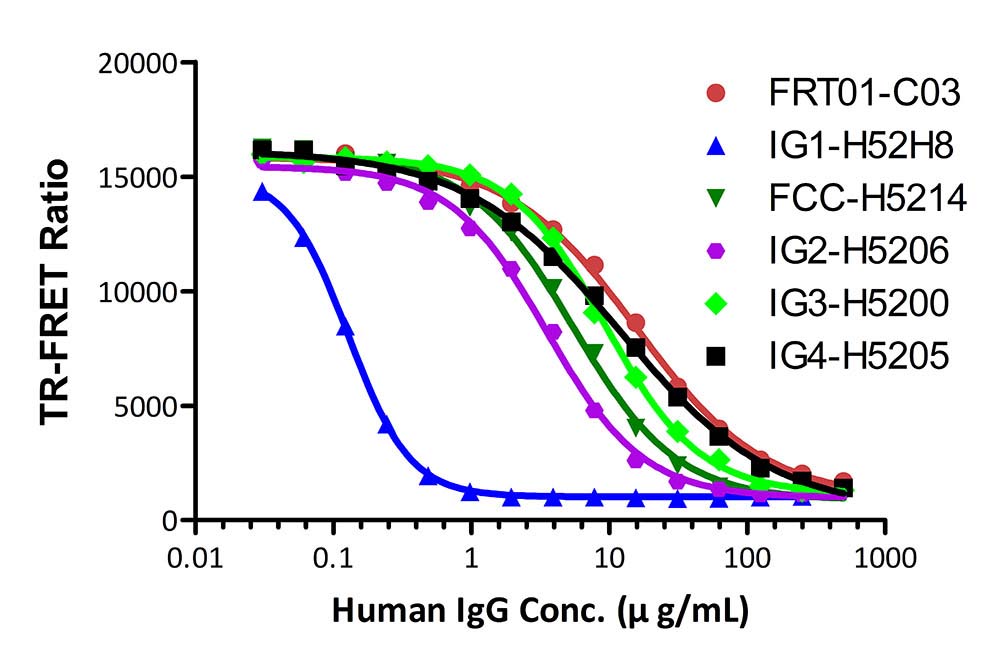
The
kit has been used to detect different human IgG isoforms of Human IgG1
Fc, Human IgG2 Fc, Human IgG3 Fc, Human IgG4 Fc, and modified Human IgG1
Fc (C103S, M135Y, S137T, T139E, H316K, N317F) Protein, His Tag (Cat.
No.IG1-H52H8) with different affinities binding to FcRn.
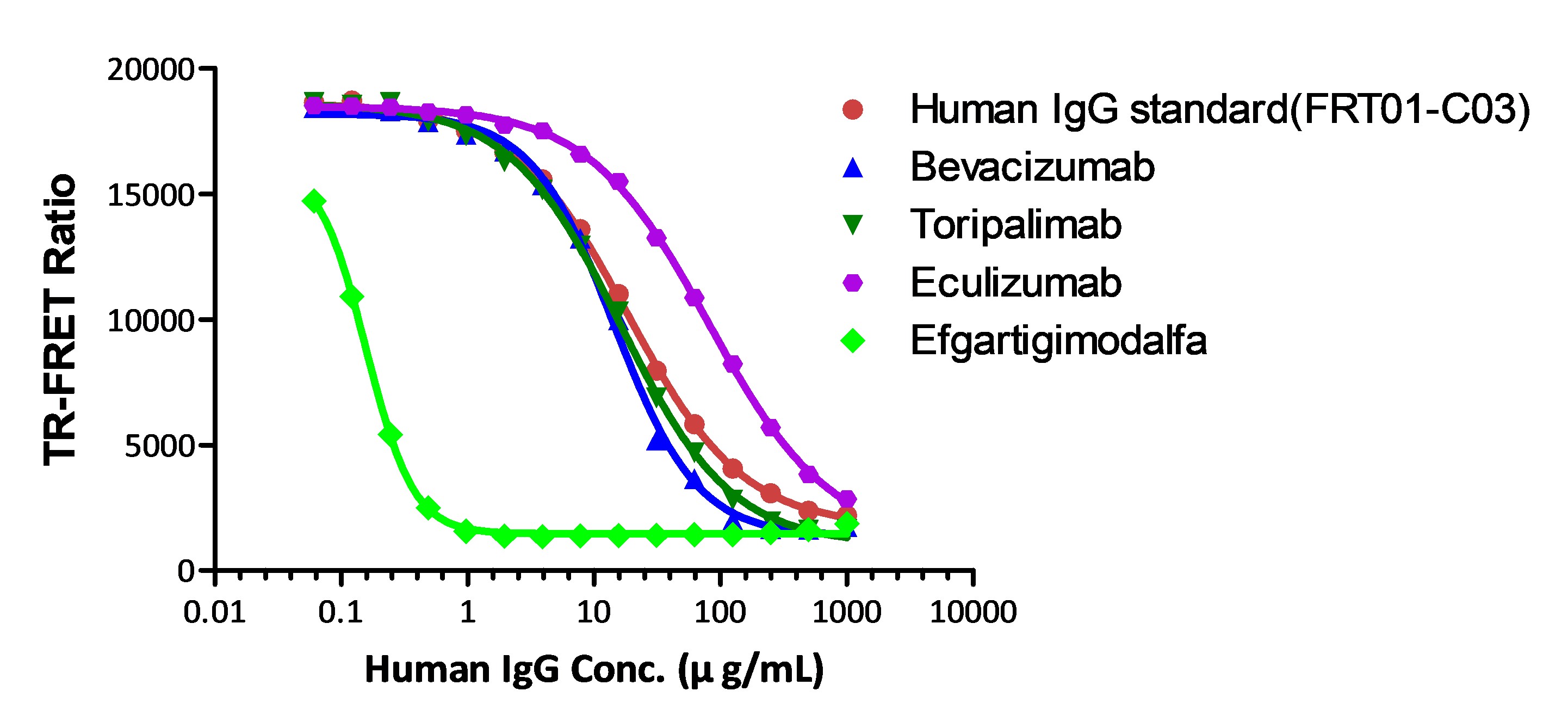
Eculizumab and Efgartigimodalfa with different affinities binding to FcRn.
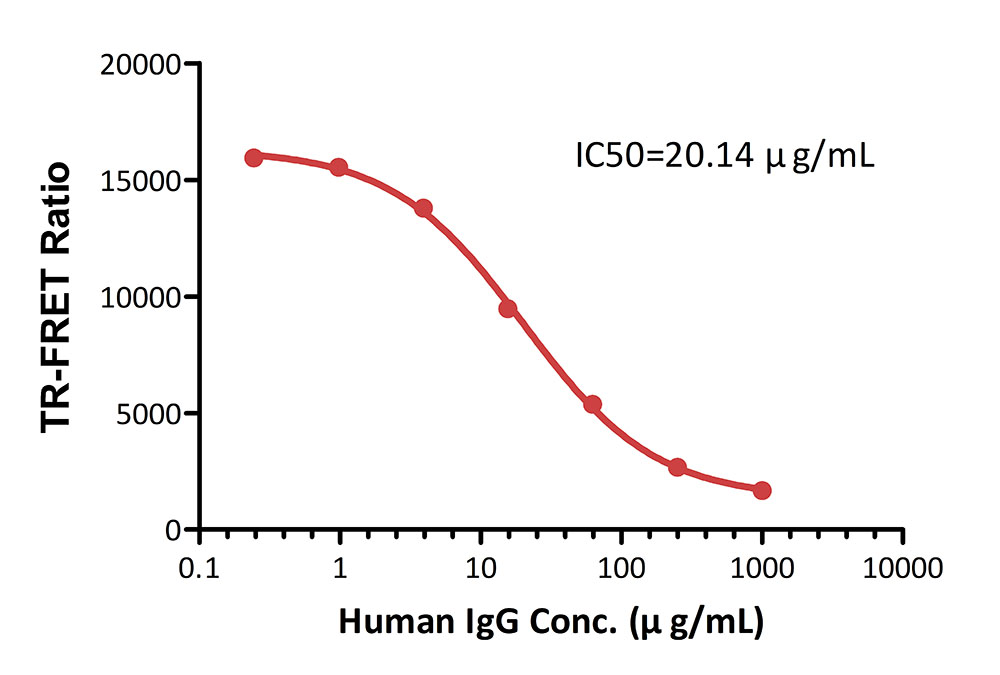
Inhibition
of Europium-chelate labeled FcRn: FA labeled human IgG antibody binding
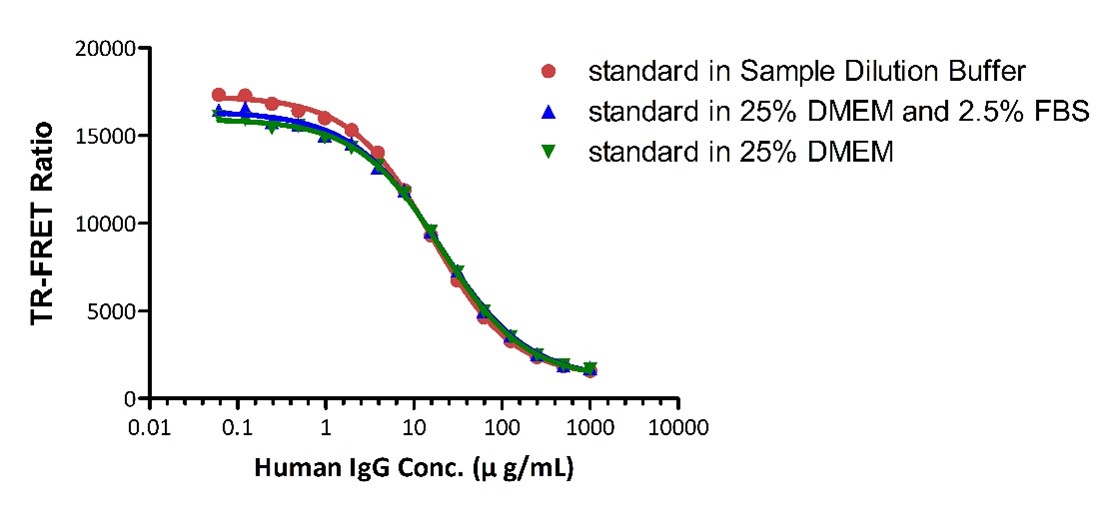
by Human IgG Premix serial dilutions of Human IgG standard (Catalog #
FRT01-C03) (1:4 serial dilution, from 1000 μg/mL to 0.24 μg/mL
(6666.67-1.63 nM)) and Human FCRN&B2M Heterodimer Protein
Europium-chelate (Catalog # FRT01-C01) and incubate at room temperature
(20℃-25℃) for 0.5 hour. Then add FA labeled human IgG antibody (Catalog #
FRT01-C02) and incubate at room temperature (20℃-25℃) for 0.5 hour.
Detection was performed with IC50 of 20.14 μg/mL.
Verify
potential matrix effects by adding different levels of DEME and FBS to
the Sample Diluted buffer. There is no effection in 25% DMEM and 2.5%
FBS
我们的重组IgG Fc蛋白仅包含了铰链区、CH2、CH3序列,不包含Fab序列,可以作为IgG结构药物(单抗、IgG样双抗、ADC、Fc融合蛋白)和FcRn靶向药物的同型对照,应用于药物筛选、功能验证等场景。
产品优势
-
HEK293细胞表达:实现翻译后糖基化修饰,确保蛋白正确折叠;
-
多种属、多亚型:Human IgG1 Fc、IgG2 Fc、IgG3 Fc、IgG4 Fc;Mouse IgG1 Fc、IgG2a Fc、IgG2b Fc;Llama IgG2b Fc,Rabbit IgG Fc;
-
多标签:Tag Free,Avitag™,His Tag,gD Tag,Flag Tag,Avitag™ &His tag;
-
严格质控,品质保证:低内毒素,经测定内毒素<1.0 EU/μg;
-
高生物活性:经ELISA&SPR验证,免费提供 Protocol。
应用数据展示
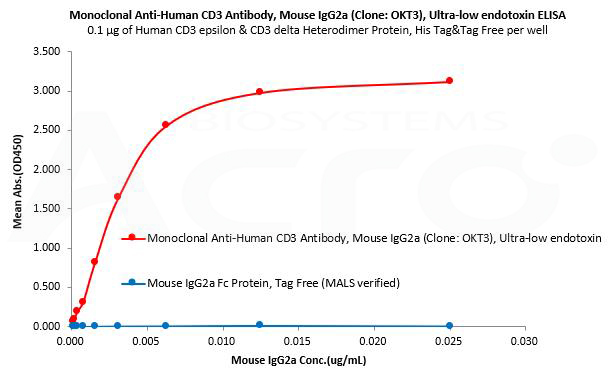
Human CD3 epsilon & CD3 delta Heterodimer Protein, His Tag&Tag Free (MALS verified) (Cat. No. CDD-H52W1) can bind Monoclonal Anti-Human CD3 Antibody, Mouse IgG2a (Clone: OKT3), Ultra-low endotoxin (Cat. No. CDE-M120a) with a linear range of 0.2-3 ng/mL and cannot bind Mouse IgG2a Fc Protein, Tag Free (MALS verified) (Cat. No.IGA-M5207).
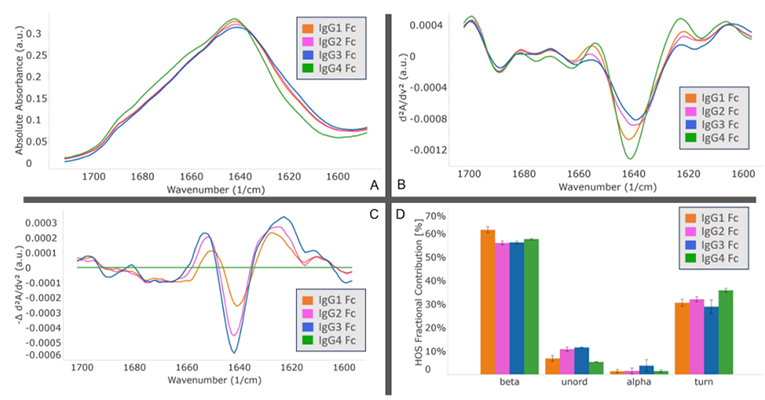
MMS
analysis showed that different IgG Fc subclasses exhibit distinct
secondary structures. Specifically, IgG1 and IgG2 exhibit the highest
degree of structural similarity, while IgG3 and IgG4 show the greatest
structural difference.
不容错过!
Human FcRn结合检测试剂盒试用装活动倒计时!

相关阅读
参考文献
1.Ulrichts
P, Guglietta A, Dreier T, et al. Neonatal Fc receptor antagonist
efgartigimod safely and sustainably reduces IgGs in humans. J Clin
Invest. 2018;128(10):4372-4386. doi:10.1172/JCI97911
2.Vaccaro
C, Zhou J, Ober RJ, Ward ES. Engineering the Fc region of
immunoglobulin G to modulate in vivo antibody levels. Nat Biotechnol.
2005;23(10):1283-1288. doi:10.1038/nbt1143
3.Hoy
SM. Rozanolixizumab: First Approval [published correction appears in
Drugs. 2023 Nov;83(16):1569. doi: 10.1007/s40265-023-01960-y]. Drugs.
2023;83(14):1341-1347. doi:10.1007/s40265-023-01933-1
4.Alabbad,
Sawsan, et al. "Monoclonal antibody-based therapies for myasthenia
gravis." BioDrugs 34 (2020): 557-566. doi: 10.1007/s40259-020-00443-w
5.Briani
C, Visentin A. Therapeutic Monoclonal Antibody Therapies in Chronic
Autoimmune Demyelinating Neuropathies. Neurotherapeutics.
2022;19(3):874-884. doi:10.1007/s13311-022-01222-x
6.抗体圈公众号






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!































 膜杰作
膜杰作 Star Staining
Star Staining