AnaptysBio大涨30%!其PD-1激动剂在RA临床2期中期数据大获成功
在竞争高度饱和的PD-1赛道,有的企业还在艰难地夹缝求生,有的企业已经找到了新方向。
2025年2月12日,AnaptysBio公司传来好消息,其开发的PD-1+T细胞耗竭剂和激动剂Rosnilimab(ANB030)在中重度类风湿关节炎(RA)的全球2b期RENOIR临床试验中取得了积极结果。结果显示,接受不同剂量Rosnilimab治疗的中重度RA患者,在DAS28-CRP(基于C反应蛋白水平的28个关节疾病活动度指数)评分方面均实现了显著改善。
这不仅是ANAB一家biotech一家小小的成功,更是PD-1激动剂在自免类型疾病的一次里程碑式的突破,也为深陷“红海”困境的企业指明了一条潜在突围路径。
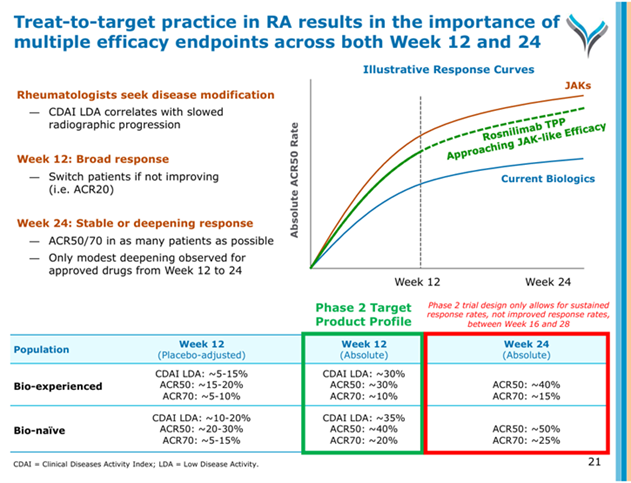
此次II期b级RENOIR研究中,纳入了424例接受过至少一种常规改善病情抗风湿药物(cDMARDs)治疗的中重度RA成人患者,评估了Rosnilimab(每四周100mg、每四周400mg或每两周600mg)对比安慰剂的疗效和安全性。
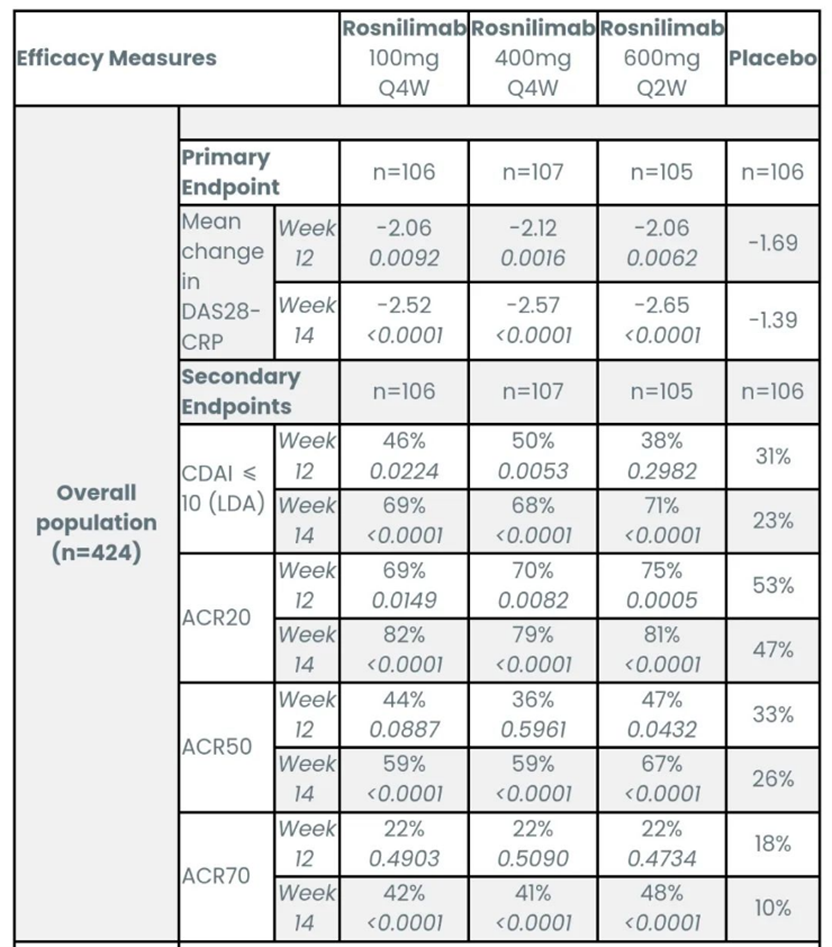
Rosnilimab在所有剂量组(100 mg、400 mg每四周一次,600 mg每两周一次)均达到主要终点,即第12周时DAS-28CRP评分较基线的平均变化较安慰剂有统计学显著差异。同时,在第12周时,Rosnilimab在至少一个剂量下达到ACR20、ACR50及CDAI低疾病活动度的关键次要终点,且所有剂量均显示数值优势。并在第14周时,响应率创新高,69%患者达CDAILDA,28周时持续响应。Rosnilimab展现强大药理学活性,显著减少PD-1high T细胞和PD-1+ T细胞,增加调节性T细胞(Tregs),调节免疫稳态。同时显著降低C反应蛋白(CRP)水平。
值得注意的是,无论是否使用过改善病情抗风湿药DMARDs,Rosnilimab在患者均获益明显,疗效优于同期JAK抑制剂乌帕替尼(ACR50约45%)。此外,Rosnilimab在安全性和耐受性方面试验中也表现得极为出色。与安慰剂相比,不良事件发生率相似。
Anaptys计划在2025年第二季度发布完整的28周数据以及更多关于类风湿关节炎的转化医学数据。Rosnilimab除了在类风湿性关节炎上进行了临床试验外,公司还计划做进一步的适应症扩展,预计在2025年第四季度发布Rosnilimab在溃疡性结肠炎(UC)2期临床试验的12周顶线数据。
PD-1的激动剂赛道——PD-1药物差异化的一扇大门
在PD-1激动剂研发领域,礼来是先行者,其开发的PD-1激动剂Peresolimab初期数据惊艳,曾被寄予厚望。2023年5月18日,礼来在N Engl J Med 期刊上刊发了Peresolimab治疗RA的临床IIa期试验结果,在这项2a期双盲、随机、安慰剂对照试验中,研究者按照2:1:1的比例将患有中重度RA的成年患者(这些患者对常规合成的抗风湿性疾病药物(DMARD)或生物或靶向合成的DMARD不应答、耐药或副作用不可耐受)分配给700 mg Peresolimab组,300mg Peresolimab组或安慰剂组,每4周静脉注射一次。
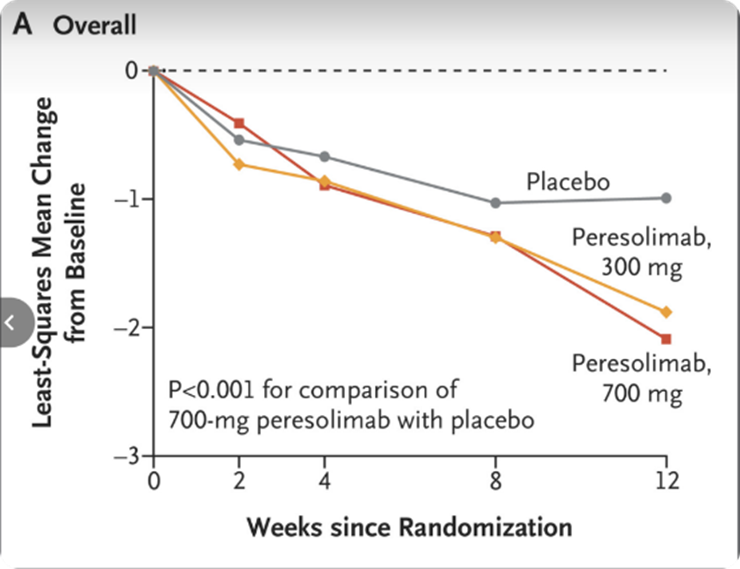
Peresolimab在RA患者的2a期试验中显示出疗效。结果显示,治疗第12周,Peresolimab(700mg,每月1次)组患者的DAS28-CRP评分较安慰剂组显著下降(-2.09 vs -0.99分,P<0.001)。此外,Peresolimab(700mg,每月1次)组和安慰剂组达到ACR20(较基线实现20%缓解)的患者比例有明显差距(71% vs 42%)。但是,本次临床试验,其ACR50(较基线缓解50%人群比例)和ACR70响应方面并无显著优势,并且在700mg组发生了一例严重不良反应——甲状腺功能减退症状,不过根据评估,与药物干预无关。
(图片来源:A Phase 2 Trial of Peresolimab for Adults with Rheumatoid Arthritis)
遗憾的是,Peresolimab最终被礼来从研发管线中移除,当时引起了市场震动,一度让行业对于PD-1激动剂的研发丧失信心。尽管如此,Peresolimab的早期成功确实为PD-1激动剂治疗自免疾病提供了重要概念验证。如今AnaptysBio的中期数据证实了自己,从目前看AnaptysBio的PD-1激动剂展现出了比JAK抑制剂还要优秀的数据。PD-1激动剂能否在自免领域获得成功,为自免领域提供一款新的治疗方案,我们拭目以待。
PD-1作为抗肿瘤靶点已经获得了突破性的进展。反之,对于免疫应答过强的自身免疫性疾病,激活PD-1信号通路便可抑制T细胞免疫,减少免疫细胞对健康组织的无差别攻击。这种机制上的反转,为PD-1药物开辟全新的应用领域提供了依据。
近年来,全球开发自免适应症的PD-(L)1产品不到20款,肿瘤赛道内卷之下,在千亿美元级别的自免疾病市场寻求突出,也不失为一种差异化的选择。
为了满足市场对PD-(L)1的相关研发需求,ACROBiosystems百普赛斯开发优化了一系列相关产品,包括高质量PD-(L)1靶点蛋白;PD-1:PD-L2 / PD-1:PD-L1 抑制剂筛选试剂盒;PD-1/PD-L1过表达细胞株;PD-1报告基因细胞株;血药浓度检测试剂盒。这一系列产品可满足从免疫、抗体筛选和表征、细胞功能验证、信号通路研究到后期的生产质控全流程,协助加速多种疾病药物的研发。
-
靶点蛋白:高纯度PD-1/PD-L蛋白;覆盖Biotin/PE等标记形式;高生物活性经ELISA/BLI等验证。
-
抑制剂筛选试剂盒:利用内部生产的生物素化PD-(L)1蛋白,采用竞争ELISA方法开发,适用于抑制剂筛选和质控放行。
-
功能细胞株:
PD-1报告基因细胞株:基于明确MOA设计,稳定传代超20代,适用于交联作用的研究、抗体药物筛选等场景。
PD-1/PD-L1过表达细胞株:表达活性经FACS验证,确保了其在研究和药物开发中的可靠性和有效性。
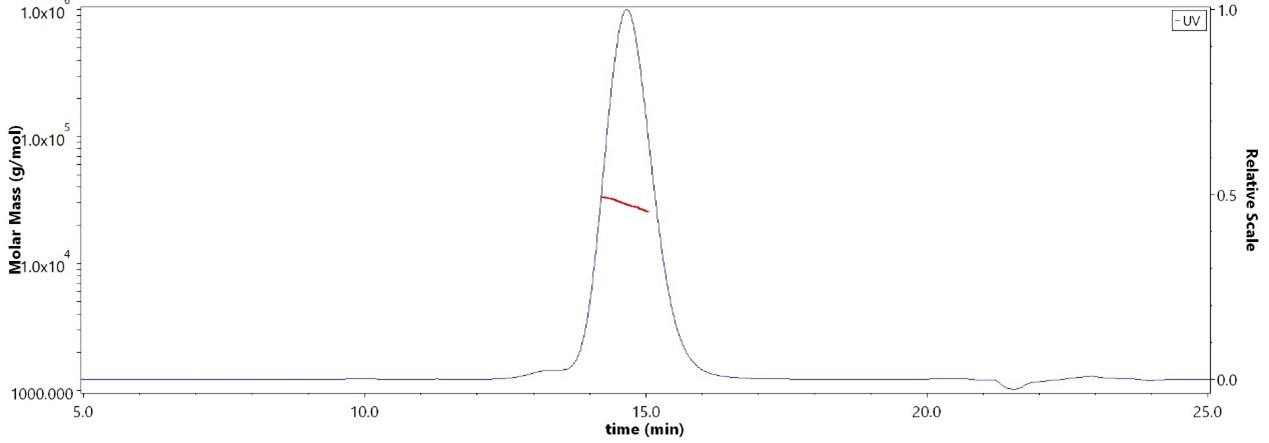
The purity of Cynomolgus PD-1, His Tag (Cat. No.PD1-C52H5) is more than 90% and the molecular weight of this protein is around 25-35 kDa verified by SEC-MALS.
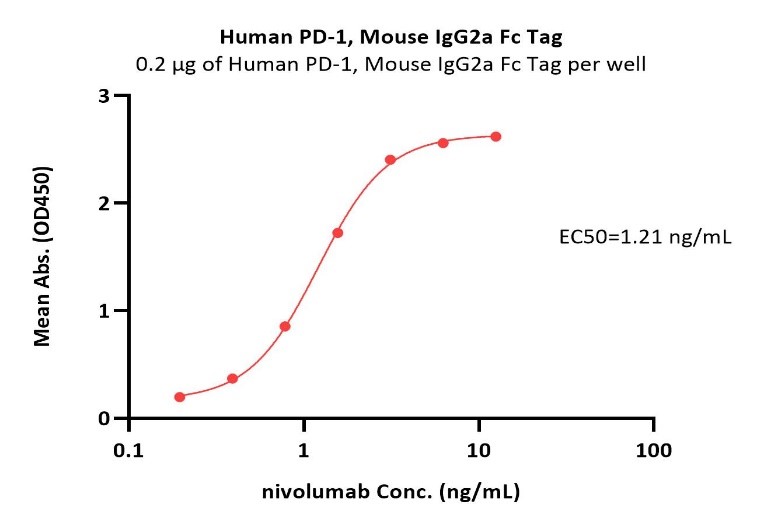
Immobilized Human PD-1, Mouse IgG2a Fc Tag (Cat. No. PD1-H5255) at 2 μg/mL (100 μL/well) can bind Nivolumab with a linear range of 0.1-2 ng/mL (Routinely tested).
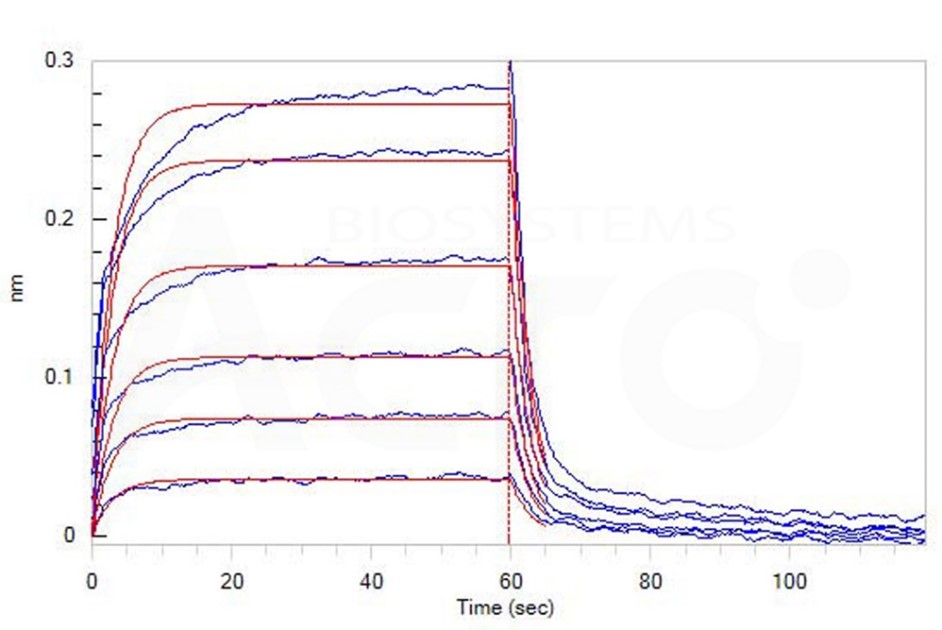
Loaded Biotinylated Human PD-1, Fc,Avitag (Cat. No. PD1-H82F1) on SA Biosensor, can bind Human PD-L1, His Tag (HPLC verified) (Cat. No. PD1-H5229) with an affinity constant of 2.5 μM as determined in BLI assay (ForteBio Octet Red96e) (Routinely tested).
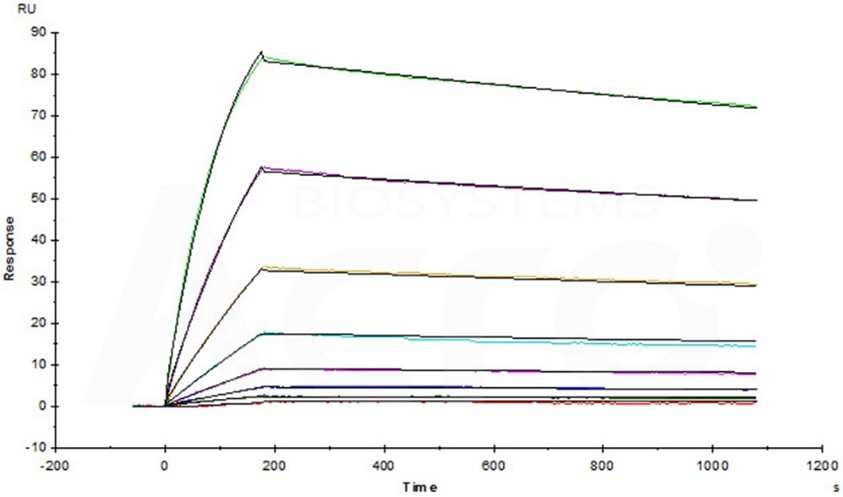
Anti-Human PD-L1 Mab (Human IgG1) captured on CM5 chip via anti-human IgG Fc antibodies surface, can bind Human PD-L1, His Tag (Cat. No. PD1-H5229) with an affinity constant of 0.286 nM as determined in a SPR assay (Biacore T200) (Routinely tested).
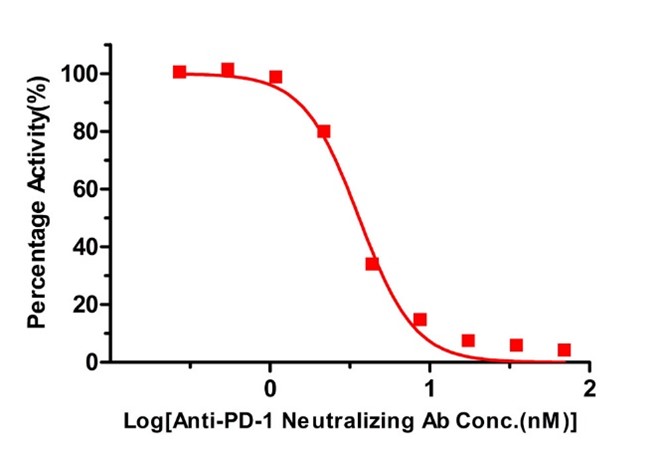
INHIBITION OF PD-1-PD-L1 BINDING BY ANTI-PD-1 NEUTRALIZING ANTIBODY (CATALOG # EP101-C03) MEASURED USING THE PD-1 [BIOTINYLATED] : PD-L1 INHIBITOR SCREENING ELISA ASSAY PAIR (CATALOG # EP-101).
Anti-PD-1 neutralizing antibody was diluted from 10 μg/mL to 0.078 μg/ mL (69.628 nM to 0.544 nM) and loaded onto the plate coated by human PD-L1 in the presence of human PD-1-Biotin. Assay was performed according to the protocol in PD-1[Biotinylated] : PD-L1 Inhibitor Screening ELISA Assay Pair. Background was subtracted from data points prior to log transformation and curve fitting (QC tested).
Human PD-1 (Luc) Jurkat Reporter Cell Development Service(Cat.No. SCJUR-STF064)
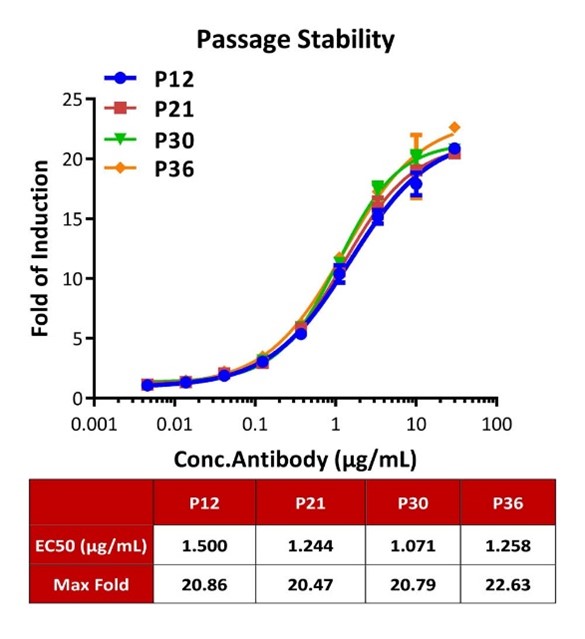
Passage stability analysis by Signaling Bioassay.
The continuously growing Human PD-1 (Luc) Jurkat Reporter Cell was stimulated with serial dilutions of Anti-human PD-1 antibody in the presence of target cells expressing human PD-L1. Anti-human PD-1 antibody stimulated response demonstrates passage stabilization (fold induction and EC50) across passage 12-36.
Human PD-1 (Luc) Jurkat Reporter Cell Development Service(Cat.No.SCJUR-STF064)
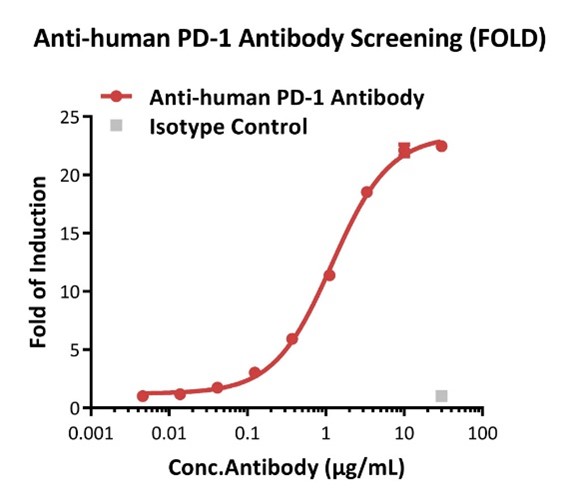
Blocking activity of anti-human PD-1 antibody (FOLD).
This reporter cell was incubated with serial dilutions of Anti-human PD-1 Antibody in the presence of target cells expressing human PD-L1. The max induction fold was approximately 22.47.
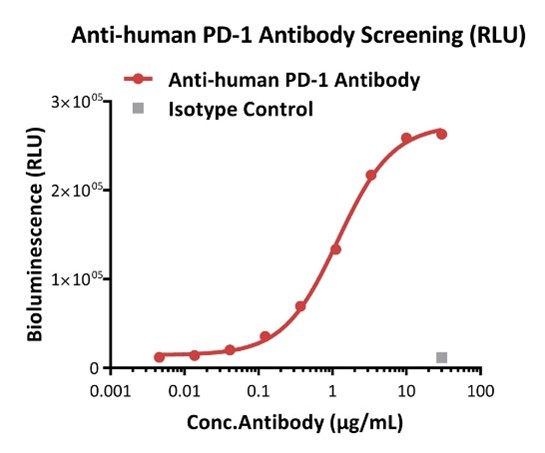
Blocking activity of anti-human PD-1 antibody (RLU).
This reporter cell was incubated with serial dilutions of Anti-human PD-1 Antibody in the presence of target cells expressing human PD-L1. The EC50 was approximately 1.189 μg/mL.






















 Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!
Star Ribbon预染蛋白Marker蛋白质标记物是生物研究和药物开发的重要组成部分。无论是用于蛋白质电泳还是western blot,我们的预染色蛋白质标记物帮助您快速确定目标蛋白质的分子量或评估转移效率。Fc受体蛋白治疗性抗体的功效取决于Fab片段及其对目标抗原的结合活性,还取决于Fc片段及其与关键Fc受体的相互作用。因此,在抗体工程中候选物必须针对一系列受体进行测试。探索我们的重组Fc受体蛋白质的全面收藏!































 膜杰作
膜杰作 Star Staining
Star Staining